


 .
.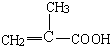 .
.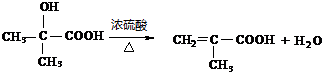
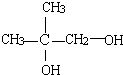
分析 由题给信息可知(CH3)2C=CH2在酸性高锰酸钾溶液中氧化生成B为 ,-CH2OH可进一步被氧化为-COOH,在浓硫酸作用下醇发生消去反应生成D为
,-CH2OH可进一步被氧化为-COOH,在浓硫酸作用下醇发生消去反应生成D为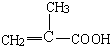 ,D和甲醇在浓硫酸作用下发生酯化反应生成E为
,D和甲醇在浓硫酸作用下发生酯化反应生成E为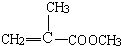 ,E中含有C=C,可发生加聚反应生成有机玻璃
,E中含有C=C,可发生加聚反应生成有机玻璃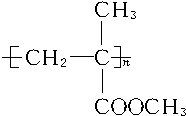 ,据此答题.
,据此答题.
解答 解:由题给信息可知(CH3)2C=CH2在酸性高锰酸钾溶液中氧化生成B为 ,-CH2OH可进一步被氧化为-COOH,在浓硫酸作用下醇发生消去反应生成D为
,-CH2OH可进一步被氧化为-COOH,在浓硫酸作用下醇发生消去反应生成D为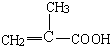 ,D和甲醇在浓硫酸作用下发生酯化反应生成E为
,D和甲醇在浓硫酸作用下发生酯化反应生成E为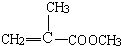 ,E中含有C=C,可发生加聚反应生成有机玻璃
,E中含有C=C,可发生加聚反应生成有机玻璃 ,
,
(1)B为 ,根据C的结构简式可知,C中含有的官能团名称分别是羟基和羧基,D为
,根据C的结构简式可知,C中含有的官能团名称分别是羟基和羧基,D为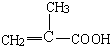 ,
,
故答案为: ;羟基;羧基;
;羟基;羧基;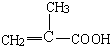 ;
;
(2)C→D的化学方程式为: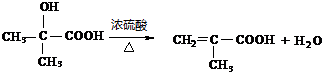 ,
,
故答案为: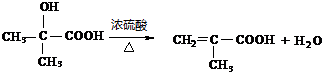 ;
;
(3)根据上面的分析可知,Y反应属于 酯化反应(或取代反应),Z反应属于加聚反应(或聚合反应),
故答案为:酯化反应(或取代反应);加聚反应(或聚合反应).
点评 本题考查有机物的推断,题目难度不大,解答本题的关键是把握相关有机物的性质,结合题给信息判断可能的反应,可推断出有机物.


 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 试管内气体呈红棕色 | B. | 试管内气体无色,是NO | ||
| C. | 试管内气体无色,是O2 | D. | 试管内液面下降 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
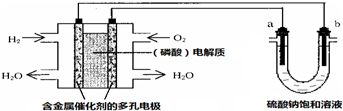
| A. | 电池工作时,正极反应式为:O2+4H++4e-═2H2O | |
| B. | 电解时,当阴极逸出amol气体,同时有W克Na2SO4﹒10H2O 析出,保持温度不变,剩余溶液中的硫酸钠的质量分数是$\frac{71W}{161(W+36a)}$×100% | |
| C. | 电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 | |
| D. | 忽略能量损耗,当电池中消耗0.01g O2时,b 极周围会产生0.02g H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,PM2.5值越高,大气污染越严重.因此由PM2.5引起的雾霾一定属于气溶胶 | |
| B. | 纪录片中详细阐述了煤的大量燃烧是产生雾霾的主要原因,如果使用前对煤进行脱硫处理,可减少二氧化硫的排放;石膏法脱硫工艺是一种常用的脱硫技术 | |
| C. | 汽车尾气中的氮氧化物和碳氢化合物在大气环境中受强烈的太阳紫外线照射后产生一种新的二次污染物--光化学烟雾也会引起雾霾,汽车尾气中含有氮氧化物,原因是汽油燃烧不充分 | |
| D. | 多植树造林,使用“乙醇汽油”,改燃煤为燃气,外出时使用PM2.5的口罩等都是治理“雾霾”等灾害性天气的有效措施 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 | |
| B. | 保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加 | |
| C. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 | |
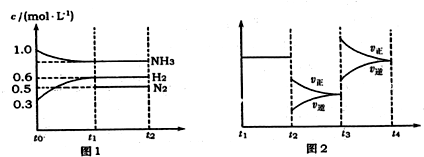
| D. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物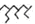 的名称为2,4 一二乙基-6-丙基辛烷 的名称为2,4 一二乙基-6-丙基辛烷 | |
| B. | 月桂烯 (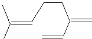 )所有碳原子一定在同一平面上 )所有碳原子一定在同一平面上 | |
| C. | 向浓醋酸溶液中加入少量碳酸钠溶液,将产生气体通入苯酚钠溶液,苯酚钠溶液中出现白色浑浊,说明酸性:醋酸>碳酸>苯酚 | |
| D. | 在盛有试粉溶液的试管中加入70%的硫酸边搅拌边加热5分钟,冷却至室温,再加入氢氧化钠中和至碱性.加入银氨溶液水浴加热,产生银镜.说明淀粉水解能产生还原性糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 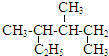 的系统命名是3,4-二甲基己烷 的系统命名是3,4-二甲基己烷 | |
| B. | 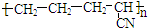 是有单体CH2=CH-CH3和CH2=CN发生加聚反应而得到的 是有单体CH2=CH-CH3和CH2=CN发生加聚反应而得到的 | |
| C. | 等质量的甲醛和乳酸[CH3CH(OH)COOH]完全燃烧消耗的氧气不相等,但生成水的质量相等 | |
| D. | 分析反应: ,由于该反应生成了不饱和化合物(含碳氧双键)和小分子,因此该反应属于消去反应 ,由于该反应生成了不饱和化合物(含碳氧双键)和小分子,因此该反应属于消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
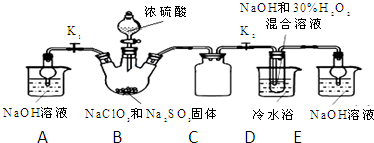
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com