
| ��� | ʵ������ | ʵ������ | ���ӷ���ʽ | ʵ����� |
| �� | ��FeCl2��Һ�е���������ˮ | ��Һ��dz��ɫ��Ϊ��ɫ | 2Fe2++Cl2=2Fe3++2Cl- | Fe2+���л�ԭ�� |
| �� | ��FeCl3��Һ�м����������� | ��Һ�ɻ�ɫ��Ϊdz��ɫ | Fe+2Fe3+=3Fe2+ | Fe3+���������� |
| �� | ��FeCl3��Һ�е�������KI��Һ�͵�����Һ | ��Һ���ձ�Ϊ��ɫ | 2Fe3++2I-�T2Fe2++I2 | Fe3+���������� |
���� ��FeCl2��Cl2��Ӧ����FeCl3��
������Һת��������Ϊ��ɫ����������Ϊdz��ɫ��Fe�������ӷ�Ӧ�����������ӣ�
�������ӵ������Դ��ڵ��ʵ⣬��������������ӷ�Ӧ���ɵ��ʵ⣬�ݴ˷�����
��� �⣺����FeCl2��Һ�е���������ˮ��FeCl2��Cl2��Ӧ����FeCl3���䷴Ӧ�����ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-��
�ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��
������Һת��������Ϊ��ɫ����������Ϊdz��ɫ����FeCl3��Һ�м����������ۣ�Fe�������ӷ�Ӧ�����������ӣ���Һ�ɻ�ɫ��Ϊdz��ɫ��
�ʴ�Ϊ����Һ�ɻ�ɫ��Ϊdz��ɫ��
�������ӵ������Դ��ڵ��ʵ⣬��FeCl3��Һ�е�������KI��Һ�͵�����Һ����������������ӷ�Ӧ���ɵ��ʵ⣬���ʵ�����������Һ�����ɫ���䷴Ӧ�����ӷ���ʽΪ��2Fe3++2I-�T2Fe2++I2��
�ʴ�Ϊ��2Fe3++2I-�T2Fe2++I2��
���� ���⿼���������仯��������ʡ����ӷ�Ӧ�����ʵļ���ȣ���Ŀ�ѶȲ�����ȷ�����ӡ��������Ӻ͵����ӵ������Լ����ʵ�ļ��鷽�����ɽ�𣬲����ڿ���ѧ���Ի���֪ʶ��Ӧ��������


 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ҩ�� | θ��ƽ | ��ϲ |
| ��Ч�ɷֵĻ�ѧʽ | Al��OH��3 | Al2Mg6��OH��16CO3•4H2O |
| ��Է������� | 78 | 530 |
| ÿƬ����Ч�ɷݵ�ҩ�� | 0.245g | 0.5g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
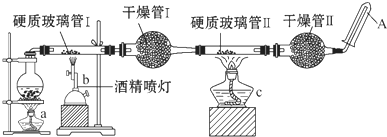 �ڳ����£�Fe��ˮ������Ӧ�����ڸ����£�Fe����ˮ����������Ӧ��Ӧ������װ�ã���̽����Ӧ�IJ��ֲ����Ӳ�ʲ����ܢ��з��뻹ԭ���ۺ�ʯ���Ļ���Ӳ�ʲ����ܢ��м���CuO������ܢ���ʢװ����������ˮ����ͭ��ʯ���Ļ����
�ڳ����£�Fe��ˮ������Ӧ�����ڸ����£�Fe����ˮ����������Ӧ��Ӧ������װ�ã���̽����Ӧ�IJ��ֲ����Ӳ�ʲ����ܢ��з��뻹ԭ���ۺ�ʯ���Ļ���Ӳ�ʲ����ܢ��м���CuO������ܢ���ʢװ����������ˮ����ͭ��ʯ���Ļ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
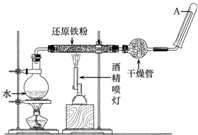 �ڳ����£�Fe��ˮ������Ӧ�����ڸ����£�Fe��ˮ�����ɷ�����Ӧ��Ӧ������װ�ã���Ӳ�ʲ������з��뻹ԭ���ۺ�ʯ���Ļ������ȣ���ͨ��ˮ�������Ϳ�����ɸ����¡�Fe��ˮ������Ӧ��ʵ�顱��
�ڳ����£�Fe��ˮ������Ӧ�����ڸ����£�Fe��ˮ�����ɷ�����Ӧ��Ӧ������װ�ã���Ӳ�ʲ������з��뻹ԭ���ۺ�ʯ���Ļ������ȣ���ͨ��ˮ�������Ϳ�����ɸ����¡�Fe��ˮ������Ӧ��ʵ�顱���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
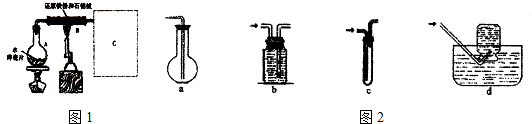
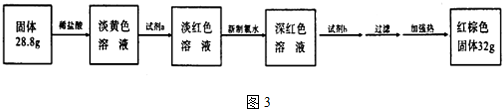
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
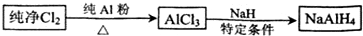
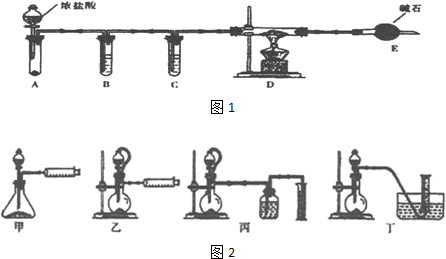
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
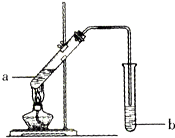 ��ͼΪʵ�����Ʊ������Ҵ�װ�ã�
��ͼΪʵ�����Ʊ������Ҵ�װ�ã�| ���� | �۵�/�� | �е�/�� | �ܶ�/g•cm-3 |
| �Ҵ� | -114 | 78 | 0.789 |
| ���� | 16.6 | 117.9 | 1.05 |
| �������� | -83.6 | 77.5 | 0.900 |
| ŨH2SO4 | 338 | 1.84 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
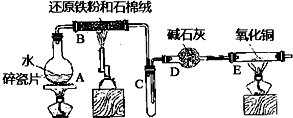
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com