
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的L层电子数为________;
(2)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为________________________________________________________________________。
科目:高中化学 来源: 题型:
CH4、H2、CO的燃烧热分别为890.31 kJ/mol、285.8 kJ/mol、110.5 kJ/mol,下列热化学方程式书写正确的是( )
A.CH4(g)+2O2(g)===CO2(g)+2H2O(g)
ΔH=-890.31 kJ/mol
B.2H2(g)+O2(g)===2H2O(l)
ΔH=-285.8 kJ/mol
C.CO(g)+H2O(g)===CO2(g)+H2(g)
ΔH=+175.3 kJ/mol
D.2CO(g)+O2(g)===2CO2(g)
ΔH=-221 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
| 温度/℃ | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
(1)①写出工业合成氨的化学方程式:________________。
②由表中数据可知该反应为放热反应,理由是________。
③理论上,为了增大平衡时H2的转化率,可采取的措施是______
(填字母序号)。
a.增大压强
b.使用合适的催化剂
c.升高温度
d.及时分离出产物中的NH3
(2)原料气H2可通过反应CH4(g)+H2O(g)CO(g)+3H2(g)获取,已知该反应中,当初始混合气中的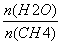 恒定时,温度、压强对平衡混合气中CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气中CH4含量的影响如图所示:
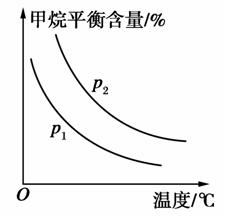
①图中,两条曲线表示压强的关系是p1________p2(填“>”、“=”或“<”)。
②该反应为________反应(填“吸热”或“放热”)。
(3)原料气H2还可通过反应CO(g)+H2O(g)CO2(g)+H2(g)获取。
①T ℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为________该温度下反应的平衡常数K值为________。
②保持温度仍为T ℃,改变水蒸气和CO的初始物质的量之比,充入容积固定为5 L的容器中进行反应,下列描述能够说明体系处于平衡状态的是________________(填字母序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n(CO)n(H2O)n(CO2)n(H2)=11666
查看答案和解析>>
科目:高中化学 来源: 题型:
判断下列说法是否正确,不正确的说明理由。
①氨气溶于水能导电,所以氨气是电解质。
②实验室用浓氨水与NaOH固体制取氨气。
③氨与酸反应生成铵盐,与挥发性酸相遇时能形成白烟。
④某晶体与NaOH共热放出一种使湿润的红色石蕊试纸变蓝的气体,该晶体中含有NH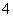 。
。
⑤氨水中含氮微粒中最多的微粒是NH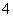 。
。
⑥把NH3通入稀HNO3中,当溶液的pH等于7时,是NH3和HNO3等物质的量反应。
⑦液氨作为清洁能源的反应原理是4NH3+5O2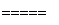 4NO+6H2O。
4NO+6H2O。
⑧氨水中物质的量浓度最大的粒子是NH3·H2O(除水)。
⑨在1 mol·L-1氨水中,NH3·H2O、NH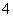 、NH3的物质的量浓度之和为1 mol·L-1。
、NH3的物质的量浓度之和为1 mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3是一种重要的化工原料,可以制备一系列物质(如图)。下列有关表述正确的是( )
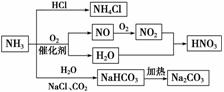
A.NH4Cl和NaHCO3都是常用的化肥
B.NH4Cl、HNO3和Na2CO3受热时都易分解
C.NH3和NO2在一定条件下可发生氧化还原反应
D.图中所涉及的盐类物质均可以水解
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气溶于水得到氨水,氯气溶于水得到氯水,下列关于新制的氨水、氯水的描述正确的是 ( )
A.“两水”都是混合物,溶液中含有的粒子种类、数目相同
B.“两水”中都存在可逆反应的化学平衡和弱电解质的电离平衡
C.“两水”都有刺激性气味,都能漂白有机色素
D.“两水”放置时间较久后,都会因为相同的原理而变质
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸铜是制备CuZnAl系催化剂的重要原料,制取硝酸铜现有三种设计方案可供选用:
①Cu与稀硝酸反应制取:3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O ②Cu与浓硝酸反应制取:Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O ③通氧气于铜屑与稀硝酸的体系中制取:2Cu+4HNO3+O2===2Cu(NO3)2+2H2O
下列说法正确的是 ( )
A.制取相同量的硝酸铜需硝酸的量③最多
B.制取相同量的硝酸铜①产生的有毒气体比②多
C. 三种方案中硝酸的利用率③>①>②
三种方案中硝酸的利用率③>①>②
D.三种方案的反应都可以在铁制容器中进行
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式表达不正确的是( )
A.碳酸钙和稀盐酸反应:CaCO3+2H+===Ca2++CO2↑+H2O
B.将磁性氧化铁溶于盐酸:Fe3O4+8H+===2Fe2++Fe3++4H2O
C.金属铝加入到NaOH溶液中:2Al+2OH-+2H2O===2AlO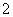 +3H2↑
+3H2↑
D.金属钠与水反应:2Na+2H2O===2Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数的值,下列说法中正确的是 ( )
①该氯原子的相对原子质量为12a/b ②m g该氯原子的物质的量为m/(aNA)mol ③该氯原子的摩尔质量是aNA g ④a g该氯原子所含的电子数为17 mol
A.①③ B.②④
C.①② D.②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com