

���� ���ݷ�Ӧ�ʱ�=��Ӧ����ѻ�ѧ�����յ�����-�������γɻ�ѧ���ų�����������õ�N-H���������յ����������ݸ�˹���ɿ��Ը�����֪��Ӧ���ʱ����δ֪��Ӧ���ʱ䣮
��� �⣺�ϳɰ���ҵ�У�3H2+N2?2NH3����Ӧ�ʱ�=��Ӧ����ѻ�ѧ�����յ�����-�������γɻ�ѧ���ų�������=3��436+945.8-6��N-H������=-92.2��N-H������=391kJ��
��֪����2H2��g��+O2��g���T2H2O��g����H=-483.6kJ/mol
��N2��g��+2O2��g���T2NO2��g����H=+67.7kJ/mol��
��Ӧ4H2��g��+2NO2��g��=N2��g��+4 H2O��g�������Ǣ١�2-�ڵõ�������4H2��g��+2NO2��g��=N2��g��+4 H2 O��g����H=��-483.6kJ/mol����2-67.7kJ/mol=-1034.9 kJ/mol��
�ʴ�Ϊ��391��4H2��g��+2NO2��g��=N2��g��+4H2O��g����H=-1034.9 kJ/mol��
���� ���⿼���˻�ѧ�������ܹ�ϵ�����жϣ��ʱ����Ӧ�ã��Ȼ�ѧ����ʽ��д��֪ʶ����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ��������� | C�� | �˵���� | D�� | ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ��Ȼ�� | C�� | ����ϩ | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ�鲽�� | ���ͻ�ʵ����� |
| ��1��ȡ9.0g�л���A����ʹ��������������ܶ�����ͬ������H2��45�� | ��1���ɴ˿�֪A����Է�������Ϊ90�� |
| ��2����9.0gA������O2�г��ȼ�գ���������λ���ͨ��Ũ���ᡢ��ʯ�ң����߷ֱ�����5.4g��13.2g�� | ��2���ɴ˿�֪A�ķ���ʽΪC3H6O3�� |
| ��3����ȡA9.0g����������NaHCO3��ĩ��Ӧ������CO2����2.24L��9.0gA�������������Ʒ�Ӧ����H2Ҳ��2.24L�����������Ϊ��״���²�ã��� | ��3���ɴ˿�֪A�к��й������У�����ṹ��ʽ��-COOH��-OH |
��4��A�ĺ˴Ź�����������ͼ�� | ��4���ɴ˿�֪A�к���4�ֲ�ͬ���ʵ���ԭ�� ��5�����ϣ�A�Ľṹ��ʽΪ  �� �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
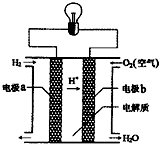
| A�� | a�缫�Ǹ��� | |
| B�� | �õ�ص��ܷ�Ӧ��2H2+O2�T2H2O | |
| C�� | ����Ϊ����Ⱦ��ˮ�����ڻ����Ѻõ�� | |
| D�� | ���·�е���b�缫ͨ����������a�缫 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��3-������ϩ�ȱ��ȶ� | |
| B�� | ����1��3-������ϩ�ȶ� | |
| C�� | 1��3-������ϩ���������ȷ�Ӧ | |
| D�� | ���������ɻ�����ķ�Ӧ��ֻ�����ʱ仯���������仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
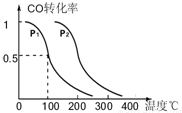
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
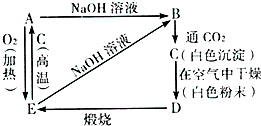 ������ͼ��Ӧ����仯���ش��й����⣮
������ͼ��Ӧ����仯���ش��й����⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH��CH | B�� | CH��C-CH3 | C�� | CH2�TCH2 | D�� | CH2�TC��CH3��CH3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com