
 .
. 分析 有机物A是芳香烃的含氧衍生物,其相对分子质量不超过130,A中含氧的质量为25.8%,可以判断B中含有氧原子数:130×25.8%÷16=2.1,所以A中含有1个氧原子,A的相对分子质量为32÷25.8%=124,(124-32)÷12=7…8,所以A的分子式为C7H8O2,
解答 解:有机物A是芳香烃的含氧衍生物,其相对分子质量不超过130,A中含氧的质量为25.8%,可以判断B中含有氧原子数:130×25.8%÷16=2.1,所以A中含有1个氧原子,A的相对分子质量为32÷25.8%=124,(124-32)÷12=7…8,所以A的分子式为C7H8O2,A苯环上的一氯代物有两种,A为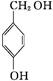 ,A有4种同分异构体
,A有4种同分异构体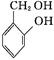 、
、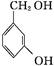 、
、
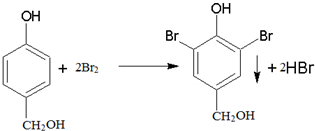
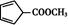 ,A与足量的浓溴水反应的化学方程式为:
,A与足量的浓溴水反应的化学方程式为: ,故答案为:C7H8O2;4;
,故答案为:C7H8O2;4; .
.
点评 本题考查有机物推断,综合分析确定A的结构是关键,做题时注意把利用好题给信息,采用正逆推相结合的方法推断,注意同分异构体的判断方法,为学习难点.


科目:高中化学 来源: 题型:多选题
| A. | NH4H中 H+的核外电子排布与He相同 | |
| B. | NH4H溶于水,所形成的溶液显碱性 | |
| C. | NH4H固体投入少量的水中,有两种气体产生 | |
| D. | NH4H与水反应时,NH4H是氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 试管编号 | 3% Na2S2O3溶液 | H2O | 稀H2SO4(体积比为1:5) | 出现浑浊时间 |
| ① | 3mL | 3mL | 5滴 | 33s |
| ② | 4mL | 2mL | 5滴 | 28s |
| ③ | 5mL | 1mL | 5滴 | cs |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
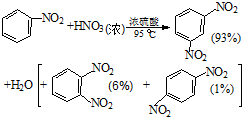
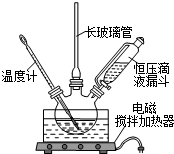 硝基苯是医药和染料的中间体,还可做有机溶剂.反应如下:
硝基苯是医药和染料的中间体,还可做有机溶剂.反应如下:
| 物质 | 熔点/ ℃ | 沸点 /℃ | 密度(20℃) /g•cm-3 | 水溶性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶 |
| 1,3二硝基苯 | 89 | 301 | 1.57 | 微溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
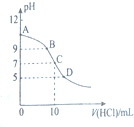 25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mLamol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )
25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mLamol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )| A. | A点溶液中加少量水,$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$减小 | |
| B. | 原氨水的物质的量浓度约为1.006×10-2mol•L-1 | |
| C. | B、D两点溶液中水电离出来的c(OH-):B<0 | |
| D. | C点溶液中的H2O不发生电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com