
| A. | 2.52 g三聚氰胺含氮原子数目为0.12NA | |
| B. | 标准状况下1 mol的三聚氰胺的体积为22.4 L | |
| C. | 三聚氰胺含氮量约为10% | |
| D. | 三聚氰胺的摩尔质量为126 |
分析 A.根据n=$\frac{m}{M}$计算三聚氰胺的物质的量,含氮原子为三聚氰胺的6倍,再根据N=nNA计算;
B.标准状况下三聚氰胺为固体;
C.化学式中某元素质量分数=(化学式中该元素原子总相对原子质量÷物质的相对分子质量)×100%;
D.摩尔质量的单位为g/mol.
解答 解:A.2.52 g三聚氰胺的物质的量为$\frac{2.52g}{126g/mol}$=0.02mol,含N原子的物质的量为0.02mol×6=0.12mol,含有N原子个数为0.12 NA,故A正确;
B.标准状况下三聚氰胺为固体,不能利用气体摩尔体积计算其体积,故B错误;
C.三聚氰胺含氮量约为$\frac{14×6}{126}$×100%=66.7%,故C错误;
D.三聚氰胺的摩尔质量为126g/mol,故D错误;
故选A.
点评 本题考查物质的量有关计算、气体摩尔体积、摩尔质量、化学式计算等,注重基础知识的考查,注意气体摩尔体积的使用条件及对象.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:解答题
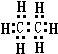 ,分子式为CmH20的烷烃中m为9,分子式为C8Hn的烷烃中n为18,与CO2 密度(同温同压)相同的烷烃分子式为C3H8.若上述四种烃各为1mol,在足量O2中燃烧,消耗O2最多的是C9H20.
,分子式为CmH20的烷烃中m为9,分子式为C8Hn的烷烃中n为18,与CO2 密度(同温同压)相同的烷烃分子式为C3H8.若上述四种烃各为1mol,在足量O2中燃烧,消耗O2最多的是C9H20.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a-b=n-m | B. | a-c=m+n | C. | c+d=m+n | D. | b-d=n-m |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +1,+3 | B. | +3,+1 | C. | +2,+3 | D. | +3,+2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
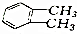 ⑥CH3CH2CH2CH(CH3)C2H5
⑥CH3CH2CH2CH(CH3)C2H5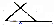 ⑧
⑧ ⑨
⑨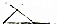
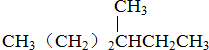
 O2
O2 ${\;}_{17}^{35}$Cl
${\;}_{17}^{35}$Cl 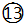 O3
O3  ${\;}_{17}^{37}$Cl
${\;}_{17}^{37}$Cl 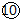 ;
; ;
;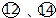 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
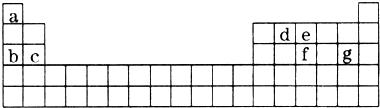
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com