
将25 mL NO2与O2的混合气体通入水后,只剩余5 mL气体,求原混合气体中NO2和O2各占多少毫升?
原混合气体中NO2和O2可能分别为16 mL和9 mL或23 mL和2 mL。
根据反应式4NO2+2H2O+O2====4HNO3,吸收后剩余气体有两种可能:①为O2,②为NO,而剩余5 mL NO是由过量NO2与H2O反应而来,所以实际过量为 15 mL NO2。
①设剩余5 mL为O2,NO2体积为x,O2总体积为y,NO2反应完。
4NO2+O2+2H2O====4HNO3
x 0.25x
依题意为![]() 解得
解得![]()
②设剩余5 mL为NO,O2用完。
4NO2+O2+2H2O====4HNO3
4y y
3NO2+H2O====2HNO3+NO
x-4y ![]()
依题意有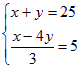 解得:
解得:![]()


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.NO2:17 mL;O2:13 mL | B.NO2:27 mL;O2:3 mL |
| C.NO2:15 mL;O2:15 mL | D.NO2:25 mL;O2:5 mL |
查看答案和解析>>
科目:高中化学 来源:2013年高考化学备考复习卷B1:非金属及其化合物(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com