
自然界中存在一种尖晶石,主要成分的化学式可表示为MgA12O4,可作为宝石.已知该尖晶石中混有Fe2O3.取5.4g样品,恰好完全溶解在100mL一定浓度的盐酸中,则该盐酸的浓度可能是()
A. 1.8mol/L B. 2.8mol/L C. 4.3mol/L D. 4.9mol/L
考点: 物质的量浓度的相关计算.
专题: 物质的量浓度和溶解度专题.
分析: 根据题意,尖晶石与盐酸反应,最终的产物是MgCl2、AlCl3、FelCl3.由于一定量样品5.4g,恰好与100mL一定浓度的盐酸反应,利用极值法进行讨论:
当全部是MgAl2O4时,与盐酸反应最终生成MgCl2和AlCl3,1mol MgAl2O4消耗8molHCl,因为恰好溶解,根据n= 计算MgAl2O4的物质的量,进而计算消耗HCl的物质的量,根据c=
计算MgAl2O4的物质的量,进而计算消耗HCl的物质的量,根据c= 计算盐酸的浓度;
计算盐酸的浓度;
假如全部是Fe2O3时,1molFe2O3消耗6molHCl,求出盐酸的物质的量浓度,实际盐酸的物质的量浓度应介于二者之间.
解答: 解:假设全部是MgAl2O4时,5.4gMgAl2O4的物质的量为 =0.038mol,与盐酸反应最终生成MgCl2和AlCl3,1mol MgAl2O4消耗8molHCl,故消耗HCl的物质的量为8mol×
=0.038mol,与盐酸反应最终生成MgCl2和AlCl3,1mol MgAl2O4消耗8molHCl,故消耗HCl的物质的量为8mol× =0.304mol,故盐酸的浓度为
=0.304mol,故盐酸的浓度为 =3.04mol/L,
=3.04mol/L,
假如全部是Fe2O3时,5.4gFe2O3的物质的量为 =0.0338mol,1molFe2O3消耗6molHCl,故消耗盐酸的物质的量为0.0338mol×6=0.203mol,故盐酸的物质的量浓度为
=0.0338mol,1molFe2O3消耗6molHCl,故消耗盐酸的物质的量为0.0338mol×6=0.203mol,故盐酸的物质的量浓度为 =2.03mol/L,
=2.03mol/L,
实际盐酸的物质的量浓度应介于二者之间,故选B.
点评: 本题考查混合物的有关计算,难度中等,利用混合物列方程进行计算,步骤繁琐而结果易错,导致费时而不易得分,注意利用极值法进行的计算.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)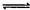 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= ;
(2)该反应为 反应(选填吸热、放热);
(3)某温度下,平衡浓度符合下式:3c(CO2)•c(H2)=5c(CO)•c(H2O),试判断此时的温度为 ℃;
(4)830℃时,向该容器中加入1L CO2与1L H2,平衡时CO2的体积分数是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
1 L稀硝酸和稀硫酸的混合液,其物质的量浓度分别为0.1 mol·L-1和0.4 mol·L-1。若向该混合液中加入足量的铜粉,则最多能溶解铜粉的质量为( )
A.2.4 g B.3.2 g
C.6.4 g D.9.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于纯净物、混合物、强电解质、弱电解质的正确组合是()
纯净物 混合物 强电解质 弱电解质 非电解质
A 纯盐酸 水煤气 硫酸 醋酸 干冰
B 冰醋酸 福尔马林 硫酸钡 亚硫酸 二氧化硫
C 油酯 淀粉 苛性钾 氢硫酸 碳酸钙
D 重水 纤维素 氯化钠 次氯酸 氯气
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是()
A. 0.1 mol•L﹣1 (NH4)2Fe(SO4)2溶液中:K+、Cu2+、Cl﹣、MnO4﹣
B. 0.1 mol•L﹣1 FeCl2溶液:K+、Na+、SO42﹣、NO3﹣
C. 使甲基橙变红色的溶液:NH4+、Cu2+、ClO﹣、Cl﹣
D. 0.1mol•L﹣1NaHCO3溶液:K+、AlO2﹣、Cl﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合物液中滴加1mol•L﹣1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断不正确的是()
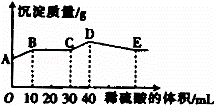
A. AB段发生反应的离子方程式为:Ba2++2OH﹣+2H++SO42﹣=BaSO4↓+2H2O
B. BC段发生反应的离子方程式为:H++OH﹣=H2O
C. D点表示的沉淀的化学式为Al(OH)3、BaSO4
D. E点表示的溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,可实现如图所示物质之间的转化.
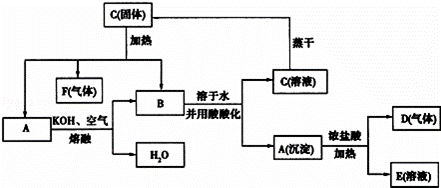
已知D为黄绿色气体,请填空:
(1)写出下列反应的化学方程式:
①C固体加热: A→B:.
(2)写出下列反应的离子方程式:
①A→D+E:;②B→C+A:.
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,向某密闭容器中投入一定量的氮气和氢气,发生反应N2(g)+3H2(g)⇌2NH3(g).下列关于从反应开始至达到化学平衡的过程中正、逆反应速率变化情况的图象中,正确的是()
A. 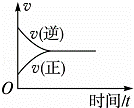 B.
B. 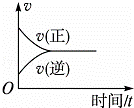 C.
C. 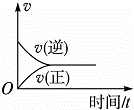 D.
D. 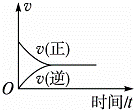
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com