
对于100mL 1mol/L盐酸与锌粒的反应,采取下列措施能使放出H2速率加快的是
①升高温度
②改用100mL 1mol/L硫酸
③多用300mL 1mol/L盐酸;
④用等量锌粉代替锌粒
⑤改用100mL 6mol/L硝酸
⑥滴入几滴硫酸铜溶液
⑦用粗锌代替纯锌使用
| A.①③④⑤⑦ | B.①②④⑥⑦ | C.②③④⑤⑥ | D.①②③⑥⑦ |
科目:高中化学 来源: 题型:单选题
对于平衡体系mA(g)+nB(g)  pC(g)+qD(g) ΔH<0。下列结论中错误的是
pC(g)+qD(g) ΔH<0。下列结论中错误的是
A.若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q
B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n
C.若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a
D.若温度不变压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
T ℃时在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图(1)所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积分数与时间的关系如图(2)所示。则下列结论正确的是( )
| A.反应进行的前3 min内,用X表示的反应速率v(X)="0.3" mol·(L·min)-1 |
B.容器中发生的反应可表示为:3X(g)+Y(g) 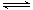 2Z(g) 2Z(g) |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| D.若改变反应条件,使反应进程如图(3)所示,则改变的条件是增大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于化学反应速率的说法正确的是
| A.化学反应速率是指单位时间内任何一种反应物物质的量的减少或任何一种生成物物质的量的增加 |
| B.化学反应速率为0.8 mol /(L·s)是指1s 时某物质的浓度为0.8mol/L |
| C.根据化学反应速率的大小可以知道化学反应进行的快慢 |
| D.决定反应速率的主要因素是反应物的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
高温下,某反应达平衡,平衡常数K=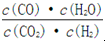 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
A 升高温度,逆反应速率减小
B.恒温恒容下,增大压强,H2浓度一定减小
C.反应的焓变为正值
D.该反应化学方程式为CO + H2O CO2+ H2
CO2+ H2
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一密闭容器中充人1mol N2和3mol H2,在一定条件下发生反应N2+3H2 2NH3,下列有关说法正确的是( )
2NH3,下列有关说法正确的是( )
| A.达到化学平衡时,正反应和逆反应的速率都为零 |
| B.当符合3u正(N2)=u正(H2)时,反应达到平衡状态 |
| C.达到化学平衡时,单位时间消耗amolN2,同时生成3amolH2 |
| D.当N2、H2、NH3的分子数比为1∶3∶2,反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在同温同压条件下,已知: C+CO2 2CO(正反应是吸热),正反应的反应速率为v1;N2+3H2
2CO(正反应是吸热),正反应的反应速率为v1;N2+3H2 2NH3(正反应是放热),正反应的反应速率为v2。对于上述反应,当温度同时升高时,v1和v2的变化情况正确的是
2NH3(正反应是放热),正反应的反应速率为v2。对于上述反应,当温度同时升高时,v1和v2的变化情况正确的是
| A.同时增大 | B.同时减小 |
| C.v1增大,v2减小 | D.v1减小,v2增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12 分)T℃时,在某容积恒为2L密闭容器中充入2molN2、4molH2,在催化剂辅助下发生反应:N2(g)+3H2(g) 2NH3(g) △H=-92.0kJ /mol。t0时刻,建立平衡后,测得生成NH3的量为2mol;从t1时刻开始,改变反应的一个条件,体系中反应速率随时间变化的情况,如下图所示。
2NH3(g) △H=-92.0kJ /mol。t0时刻,建立平衡后,测得生成NH3的量为2mol;从t1时刻开始,改变反应的一个条件,体系中反应速率随时间变化的情况,如下图所示。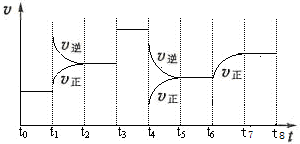
试回答下列问题:
(1)T℃时,N2的转化率为:___________,该反应的平衡常数K=___________。
(2)T℃时,下列能证明该反应已经建立平衡状态的是:__________________。
| A.体系总压强不再改变 |
| B.混合气体颜色不再改变 |
| C.H2的质量百分含量不再改变 |
| D.c(N2)与c(NH3)的比值不再改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com