
| A. | ③④⑤ | B. | ④⑤⑦ | C. | ④⑤ | D. | ③④⑤⑦ |
分析 7中物质都属于烃,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的有机物一般应具有还原性,往往应含有不饱和键,以此解答该题.
解答 解:①甲烷为饱和烃,不能与酸性高锰酸钾溶液和溴水反应,故①错误;
②苯不能与酸性高锰酸钾溶液和溴水反应,故②错误;
③聚乙烯不含不饱和键,不能与酸性高锰酸钾溶液和溴水反应,故③错误;
④1,3-戊二烯含有碳碳双键,可既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,故④正确;
⑤2-丁炔含有不饱和键,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,故⑤正确;
⑥甲苯,既不能使酸性高锰酸钾溶液褪色又不能与溴水发生反应使之褪色,故⑥错误;
⑦环己烯含有不饱和键,既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色,故⑦正确.
故选B.
点评 本题考查有机物的结构和性质,题目难度不大,注意把握有机物官能团或基团的性质,性质官能团的性质解答该题.


科目:高中化学 来源: 题型:多选题
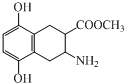
| A. | 该有机物的分子式为C12H14NO4 | |
| B. | 该有机物既可与盐酸反应,又可与NaOH溶液反应 | |
| C. | 该有机物中含有2个手性碳原子 | |
| D. | 1mol该有机物最多只能与1molBr2发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
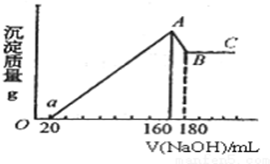 将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.
将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol苯乙烯( )中含有的C=C数为4NA )中含有的C=C数为4NA | |
| B. | 在标准状况下,11.2 L己烷含有分子数为0.5NA | |
| C. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | |
| D. | 1mol甲基含10NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S2Cl2的结构简式:S-Cl-S-Cl | |
| B. | 13.5g S2Cl2和NaOH反应电子转移数为0.1NA | |
| C. | S2Cl2和NaOH水溶液反应,氧化与还原产物物质的量之比为1:1 | |
| D. | S2Cl2和水反应中,氧化剂还原剂物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44.8L | B. | 5L | C. | 11.2L | D. | 33.6L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A2)=1.5 mol/(L•s) | B. | v(B2)=2.4 mol/(L•s) | C. | v(C)=1.6 mol/(L•s) | D. | v(A2)=6 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

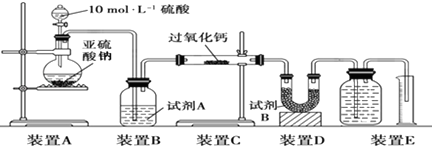
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com