
【题目】下列各组元素性质递变错误的是
A.Li、Be、B原子最外层电子数逐渐增多B.N、O、F氢化物的稳定性依次减弱
C.P、S、Cl最高正价依次升高D.Li、Na、K的金属性依次增强
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】由乙烯推测丙烯的结构或性质正确的是( )
A.分子中所有原子在同一平面上B.与HCl加成只生成一种产物
C.能使KMnO4酸性溶液褪色D.能与溴水发生取代反应而使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,由水电离的c(H+)=1.0×l0-13mol/L的溶液中一定不可能大量存在的离子是
A. NH4+ B. HCO3- C. OH- D. Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将224.00L氯化氢气体溶于635.00mL的水(密度为1.00g/cm3)中,所得盐酸的密度为1.18g/cm3 . (要求有解题过程)
(1)该盐酸的质量分数是多少?
(2)取这种盐酸100.00mL,稀释到500.00mL,所得的稀盐酸的物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)氧化铜矿用稀硫酸溶解后所得酸浸液(含Cu2+、H+、SO42﹣、Mg2+、A13+、Fe2+) 经下列流程可制得高纯度硫酸铜晶体如图1: 
已知:该实验条件下,各金属离子沉淀的pH如图2所示.下列判断正确的是( )
A.沉淀1的主要成分为Al(OH)3和Fe(OH)3
B.溶液2中所含金属阳离子只有Mg2+
C.将溶液3蒸干即得CuSO45H2O晶体
D.若不加入NaClO溶液,对制得硫酸铜晶体的纯度将无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)是一种重要的液态火箭燃料,具有弱碱性和强还原性.工业上利用尿素[CO(NH2)2]、NaC1O在NaOH溶液中发生反应生成水合肼(N2H4H2O)、Na2CO3等产物.请回答:
(1)上述生成水合肼的反应中尿素是( 填“氧化剂”或“还原剂”),反应的化学方程式为 .
(2)肼与盐酸反应可生成N2H6C12 , N2H6C12的水溶液显性( 填“酸”或“碱”或“中”),用离子方程式表示其原因 .
(3)查资料得,在高温下肼可将锅炉内壁表面的铁锈转化为致密的氧化膜.取3.2g肼与96g该铁锈样品(可看作是Fe2O3)在高温下恰好完全反应生成氮气等产物,写出该反应的化学方程式 .
若要设计实验方案检验上述反应生成固体产物中的金属离子,补充完整下列实验步骤:
①所得固体溶入浓盐酸中;
②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为( )
A.![]()
B.(2b﹣a)mol/L
C.![]()
D.(10b﹣5a)mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X,Y,Z,W,Q在元素周期表中的相对位置如图所示.下列说法正确的是( ) 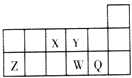
A.原子半径Y<Z<W
B.元素Y的最高正化合价比元素X的最高正化合价高
C.元素W的最高价氧化物对应的水化物的酸性比Q的弱
D.元素X的气态氢化物的稳定性大于元素Y的气态氢化物的稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.所有不锈钢都只含有金属元素
B.我国流通的硬币材质是金属单质
C.广东打捞的明代沉船上存在大量铝制餐具
D.镁合金的硬度和强度均高于纯镁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com