


科目:高中化学 来源: 题型:
| A、石灰石溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、向NaAlO2溶液中通入少量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| C、过量的二氧化碳与氢氧化钠反应:CO2+OH-=HCO3- |
| D、少量的氢氧化钠和碳酸氢钙反应:Ca2++2HCO3-+OH-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
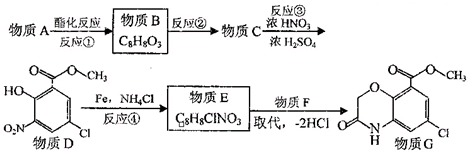
查看答案和解析>>
科目:高中化学 来源: 题型:
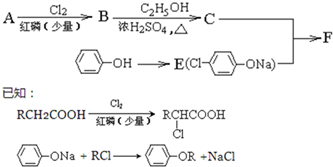
| NaOHC2H5OH |
| △ |
| 一定条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:
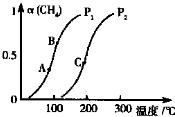 天然气在工农业生产中具有重要意义.
天然气在工农业生产中具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
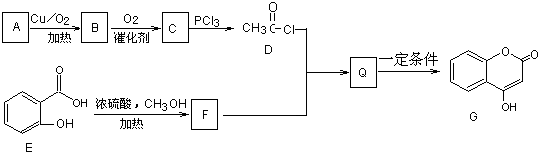
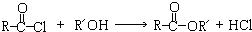
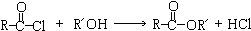 .
.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用活性炭去除冰箱中的异味 |
| B、用热碱水清除炊具上残留的油污 |
| C、用浸泡过高锰酸钾溶液的硅藻土保存水果 |
| D、用含碱石灰的透气小袋与食品一起密封包装 |
查看答案和解析>>
科目:高中化学 来源: 题型:
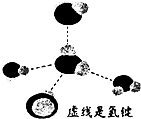 元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,
元素X、Y、Z、Q、W原子序数依次增大,其中X、Y、Z、Q为短周期元素.Z元素的焰色反应为黄色;X与Y形成的气体能使酚酞溶液变红,X与Q形成18电子的分子,查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com