
����Ŀ����ˮ���̲��ŷḻ����Դ����ˮ�ۺ����õIJ�������ͼ���£�
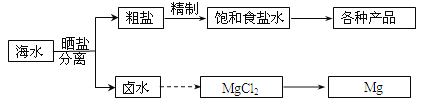
�ش��������⣺
��1����NaCl��ԭ�Ͽ��Եõ����ֲ�Ʒ
�ٹ�ҵ����NaCl�Ʊ������ƵĻ�ѧ����ʽ��________________��
��ʵ�����ö��Ե缫���200mLNaCl��Һ���������������õ�224mL���壨��״��������������Һ��pHΪ_________�����Է�Ӧǰ����Һ������仯����
�۵���Ȼ���ϡ��Һ���Ʊ���84������Һ����84������Һ����Ч�ɷ�Ϊ______����ȡ���Ļ�ѧ����ʽΪ__________________________��
��2����������κ��±ˮ���̺��ŷḻ��þ��Դ����ת����ɻ��MgCl2�ֲ�Ʒ����±ˮ����ȡþ�IJ���Ϊ��
a�������ߴ������ڵı������ճ�ʯ�ң�����ʯ���Ƴ�ʯ���飻
b����ʯ������뵽��ˮ�������о����˵õ�Mg(OH)2������
c����Mg(OH)2�����м�������õ�MgCl2��Һ���پ������ᾧ�õ�MgCl26H2O��
d����MgCl26H2O��һ�������¿��Եõ���ˮMgCl2��
e��������ڵ�MgCl2�ɵõ�Mg��
��������ȡþ������c�У��õ�MgCl2��Һ�����ӷ���ʽΪ______________��
�ڲ���d�е���һ��������ָ����___________________��
����ͬѧ��Ϊ������b��ɼ���Mg(OH)2�õ�MgO���ٵ�����ڵ�MgO�ƽ���þ�������ɼ�ʵ�鲽�裬����ʵ��ļ�Լ��ԭ����ͬ���ͬѧ���뷨��__________������ͬ����������ͬ����������˵����ͬ���ͬ�������______________��
���𰸡�2NaCl�����ڣ�![]() 2Na+Cl2�� 13 NaClO NaCl+H2O
2Na+Cl2�� 13 NaClO NaCl+H2O![]() NaClO+H2�� Mg(OH)2+2H+= Mg2++2H2O ��HCl�����м��� ��ͬ�� ��ΪMgO�۵�ܸߣ�����ʱ�����Ĵ����ĵ��ܶ����������ɱ�
NaClO+H2�� Mg(OH)2+2H+= Mg2++2H2O ��HCl�����м��� ��ͬ�� ��ΪMgO�۵�ܸߣ�����ʱ�����Ĵ����ĵ��ܶ����������ɱ�
��������
��1�������ƱȽϻ��ã���ȡʱֻ�ܲ��õ��ķ���������ʽΪ��2NaCl�����ڣ�![]() 2Na+Cl2�����ڵ�ⱥ��ʳ��ˮ�������õ������������õ����������������ʵ���Ϊ��
2Na+Cl2�����ڵ�ⱥ��ʳ��ˮ�������õ������������õ����������������ʵ���Ϊ��![]() =0.005mol����2NaCl+2H2O
=0.005mol����2NaCl+2H2O![]() Cl2��+H2��+2NaOH ��֪��Cl2����H2����2NaOH����n��NaOH��=2n��Cl2��=2��0.005mol=0.01mol��c��NaOH��=
Cl2��+H2��+2NaOH ��֪��Cl2����H2����2NaOH����n��NaOH��=2n��Cl2��=2��0.005mol=0.01mol��c��NaOH��=![]() =0.1mol/L������pH=13��
=0.1mol/L������pH=13��
����84������ҺΪ����������Һ������Ȼ�����Һ��ȡ�������Ƶķ���ʽΪ��NaCl+H2O![]() NaClO+H2��
NaClO+H2��
��2������Mg(OH)2�����м�������õ�MgCl2��Һ��������Ӧ�����ӷ���ʽΪMg(OH)2+2H+= Mg2++2H2O��
��MgCl26H2O��һ�������¼��ȵõ���ˮMgCl2����ֱ�Ӽ���MgCl26H2O����ٽ�Mg2+ˮ�⣬�ò�����ˮMgCl2����Mg2+ˮ������ԣ�����������Ȼ��������п�����Mg2+ˮ�⣬��һ������Ϊ��HCl�����У�Ŀ��������Mg2+ˮ�⣻
������þ�۵�ܸߣ�����ʱ�����Ĵ����ĵ��ܶ����������ɱ����ʲ�ͬ���ͬѧ���뷨��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Ȥ�С���������ʼ�Ļ��䣬��Ƴ�һ��ƽ��ħ��������ͼ��ʾ��
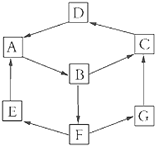
��֪��A��B��C��D��G����ͬ��Ԫ�ء�
��
��A(����) | B��Һ | D���� | G��Һ | |
��ɫ | ����ɫ | ��ɫ | ����ɫ | dz��ɫ |
��E��ͨ��������ܶ���С�����壻B����������Һ��Ӧ���ɲ�����ϡ����İ�ɫ������Ҳ�ܽ�һ������������ΪF��F�Ǻ�������Ԫ�صĻ������A��Ӧ����E��G��
����������Ϣ��գ�
(1)д��D�Ļ�ѧʽ��___________________________________________��
(2)G����C�Ĺ����������ֵ�����Ϊ_________________________��
(3)д����ӦA��B�Ļ�ѧ����ʽ��_________________________________��
(4)B��F�����ӷ���ʽΪ________��G������ᷴӦ�����ӷ���ʽΪ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B������Һ�ֱ�������ʮ�������еĸ�����ͬ�����֣�H+��Al3+��Na+��Cu2+��![]() ��OH-��
��OH-��![]() ��
��![]() ��
��![]() ��Cl-�������ж���ȷ���ǣ�������
��Cl-�������ж���ȷ���ǣ�������
A.��A��ҺΪ��ɫ��Һ����A��Һ�п��ܺ��У�H+��Al3+��Cl-��![]() ��
��![]()
B.��A��Һ��ǿ��ԭ�ԣ���B��Һ�п��ܺ��У�H+��Cu2+��Al3+��Cl-��![]()
C.��B��Һ��ǿ���ԣ���A��Һ�п��ܺ��У�H+��Al3+��Na+��Cu2+��![]()
D.��B��Һ��ǿ�������Ҹ�����Ũ����ͬ����B��Һ���ܺ��У�H+��Al3+��Cu2+��![]() ��
��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ҩ���ƿ���ç����Ϊԭ�����ϳɡ�ç����ṹ��ʽ��ͼ��ʾ������˵����ȷ����

A��ç����Ļ�ѧʽΪC7H6O5
B��1molç��������ܺ�4molNaOH������Ӧ
C��ç�������������̼ԭ�ӹ�ƽ��
D��ç������һ�������¿��Է���ȡ�����ӳɡ���ȥ��������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʳ��ά����ͻ���ı������ܣ�������ġ�����Ӫ���ء���ľ������һ�ַ�������ʳ��ά���䵥��֮һ�ǽ��Ӵ����ṹ��ʽ��ͼ��ʾ�������йؽ��Ӵ���˵����ȷ����(����)
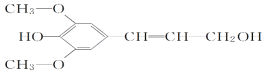
A. ���Ӵ��ķ���ʽ��C11H14O4�����ڷ�����
B. 1 mol���Ӵ�������Ũ��ˮ��Ӧ���������3 mol Br2
C. ���Ӵ�������FeCl3��Һ������ɫ��Ӧ
D. ���Ӵ��ܷ����ķ�Ӧ������������Ӧ��ȡ����Ӧ���ӳɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����в�����SO2��NOֱ���ŷŽ��Դ������������Ⱦ�����õ绯ѧԭ������SO2��NO��ͬʱ��� Na2S2O4�� NH4NO3��Ʒ�Ĺ�������ͼ���£�CeΪ��Ԫ�أ���

��ش��������⣮
��1��װ������NO����������������NO2-�����ӷ���ʽ______��
��2�����������H2SO3��![]() ��
��![]() ��������SO2��NaOH��Һ��Ӧ�����Һ�У����ǵ����ʵ�������������ҺpH�Ĺ�ϵ��ͼ1��ʾ��
��������SO2��NaOH��Һ��Ӧ�����Һ�У����ǵ����ʵ�������������ҺpH�Ĺ�ϵ��ͼ1��ʾ��
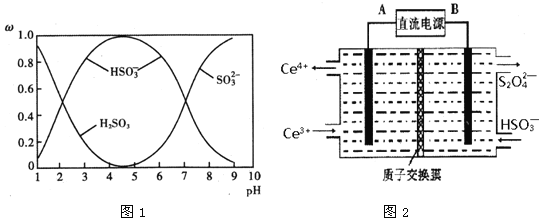
������˵����ȷ����______�����ţ���
A��pH=7ʱ����Һ��c��Na+��=3c��![]() ��
��
B����ͼ�����ݣ����Թ����H2SO3�ĵڶ�������ƽ�ⳣ��Ka2��10-7
C��Ϊ��þ����ܴ��� NaHSO3��Ӧ����Һ��pH������ 4��5Ϊ��
D��pH=9ʱ��Һ��c��OH-��=c��H+��+c��![]() ��+c��H2SO3��
��+c��H2SO3��
����1L1mol/L��NaOH��Һ��ȫ����13.44L������£�SO2����Ӧ�������ӷ���ʽΪ______��
��ȡװ�����е�����ҺVmL����cmol/L�����Ը��������Һ�ζ������Ը��������ҺӦװ��______��������ʽ��������ʽ�����ζ����У��жϵζ��յ�ķ�����______
��3��װ����������֮һ������Ce4+����ԭ����ͼ2��ʾ��ͼ��AΪ��Դ��______�������������������������Ҳ෴Ӧ���з�������Ҫ�缫��ӦʽΪ______��
��4����֪����װ��������Һ��NO2-��Ũ��Ϊ 0.4mol/L��Ҫʹ 1m3����Һ�е�NO2-��ȫת��Ϊ NH4NO3����������װ������ͨ���״���µ� O2�����Ϊ______ L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����⣨PH3����һ�־綾���壬�dz��õĸ�ЧѬ��ɱ�����Ҳ��һ�ֵ��ӹ�ҵԭ�ϣ�
��1�����ܱ����ַ��õ�������AIP��Ƭ������ˮ�����ų�PH3���壬��ѧ����ʽΪ ______
��2�����÷�ӦPH3+3HgCl2=P(HgCl)3��+3HCl��ͨ���ⶨ��Һ ______ �仯����ȷ�ⶨ����������PH3������HgCl2����ˮ��������Һ���������磬��HgCl2���� ______ �����������������������������
��3����ҵ�Ʊ�PH3��������ͼ1��ʾ��

������������ ______ Ԫ�
������ӦI���ɵ�n��NaH2PO2����n��Na2HPO3��=3��1ʱ���μӷ�Ӧ��n��P4����n��NaOH��= ______ ��
��4����Ư�ۿɽ�PH3����ΪH3PO4����ѧ����ʽΪ ______ ������ˮ����ʱ�ɼӿ�PH3���������̣������ӷ���ʽ��ʾԭ�� ______ ��
��5���ӣ�4���еķ�Ӧ�����л���������ƣ�CaHPO4���ķ�����ͼ2��
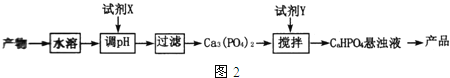
���Լ�XΪ ______ ���ѧʽ����
����֪25��ʱ��H3PO4��Ka1=7.5��10-3��Ka2=6.3��10-8��Ka3=4.4��10-13��
CaHPO4����ҺpH ______ 7��������������=��������������ͨ������˵������ ______ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȡ���кܸߵ�ҩ�ü�ֵ����ԭ��(��ͼ),����˵���������

A.1 mol��ԭ����������ˮ��Ӧ,�������4 mol Br2
B.��ԭ���ܷ���ȡ�����ӳɡ���ȥ��������Ӧ
C.1 mol��ԭ��������Na��Ӧ���������ڱ���µ����Ϊ33.6L
D.��ԭ��ˮ���һ�ֲ�������FeCl3������ɫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������˵��2HI��g��H2��g��+I2��g���Ѵ�ƽ��״̬����__________
�ٵ�λʱ��������nmolH2��ͬʱ������nmolHI��
��1��H��H�����ѵ�ͬʱ��2��H��I�����ѣ�
�ۻ�����аٷ����ΪHI%=I2%��
�ܷ�Ӧ����v��H2��=v��I2��=![]() v��HI��ʱ��
v��HI��ʱ��
�ݻ��������c��HI����c��H2����c��I2��=2��1��1ʱ��
���¶Ⱥ����һ��ʱ��ijһ������Ũ�Ȳ��ٱ仯��
���¶Ⱥ����һ��ʱ��������ѹǿ���ٱ仯��
������һ������������ƽ�������������ٱ仯��
���¶Ⱥ����һ��ʱ������������ɫ���ٱ仯��
���¶Ⱥ�ѹǿһ��ʱ�����������ܶȲ��ٱ仯��
�����ޡ����˵������˵��2NO2N2O4�ﵽƽ��״̬����___________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com