
ĻąĶ¬ĪĀ¶ČĻĀ£¬100 mL 0.01 mol”¤L£1µÄ“×ĖįČÜŅŗÓė10 mL 0.1 mol”¤L£1µÄ“×ĖįČÜŅŗĻą±Č½Ļ£¬ĻĀĮŠŹżÖµĒ°Õß“óÓŚŗóÕߵďĒ( )
A£®c(OH£) B£®c(H£«) C£®ÖŠŗĶŹ±ĖłŠčNaOHµÄĮæ D£®c(CH3COOH)
”¾“š°ø”æA
”¾½āĪö”æÓÉn=cVæÉÖŖ£¬100 mL 0.01 mol/LµÄ“×ĖįČÜŅŗÖŠČÜÖŹµÄĪļÖŹµÄĮæĪŖ0.001 mol£¬10 mL0.1 mol/LµÄ“×ĖįČÜŅŗÖŠČÜÖŹµÄĪļÖŹµÄĮæĪŖ0.001 mol£¬µ«ŗóÕßµÄÅØ¶Č“ó£¬“×ĖįµÄµēĄė³Ģ¶ČŠ”£¬ĖłŅŌĒāŃõøłĄė×ÓµÄĪļÖŹµÄĮæÅضČĒ°Õß“óÓŚŗóÕߣ¬ĒāĄė×ÓÅضČĒ°Õߊ”ÓŚŗóÕߣ¬AÕżČ·£¬B“ķĪó£»C£®ÓÉÓŚČÜÖŹn(CH3COOH)¶¼ĪŖ0.001 mol£¬ÖŠŗĶŹ±ĖłŠčNaOHµÄĮæÓ¦ĻąĶ¬£¬“ķĪó£»D£®ÓÉn=cVæÉÖŖ£¬100 mL 0.01 mol/LµÄ“×ĖįČÜŅŗÖŠČÜÖŹµÄĪļÖŹµÄĮæĪŖ0.001 mol£¬10 mL0.1 mol/LµÄ“×ĖįČÜŅŗÖŠČÜÖŹµÄĪļÖŹµÄĮæĪŖ0.001 mol£¬µ«Ē°ÕßÅØ¶ČŠ”£¬µēĄė³Ģ¶Č“ó£¬Ē°ÕßµÄCH3COOHµÄĪļÖŹµÄĮ抔£¬“ķĪó£»Ń”A”£


 ½š²©ŹæŅ»µćČ«ĶØĻµĮŠ“š°ø
½š²©ŹæŅ»µćČ«ĶØĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŌĻĀ½ųŠŠŠŌÖŹ±Č½ĻµÄŹµŃ飬²»ŗĻĄķµÄŹĒ£Ø””””£©
| ”” | A£® | ±Č½ĻCu”¢Fe2+µÄ»¹ŌŠŌ£ŗĢś¼ÓČėĮņĖįĶČÜŅŗÖŠ |
| ”” | B£® | ±Č½ĻĀČ”¢äåµ„ÖŹµÄŃõ»ÆŠŌ£ŗäå»ÆÄĘČÜŅŗÖŠĶØČėĀČĘų |
| ”” | C£® | ±Č½ĻĆ¾”¢ĀĮ½šŹōŠŌ£ŗĀČ»ÆĆ¾”¢ĀČ»ÆĀĮČÜŅŗÖŠ·Ö±š¼ÓČė¹żĮæµÄNaOHČÜŅŗ |
| ”” | D£® | ±Č½ĻĢ¼”¢Įņ·Ē½šŹōŠŌ£ŗ²ā¶ØĶ¬Ģõ¼žĶ¬ĪļÖŹµÄĮæÅØ¶ČµÄNa2CO3”¢Na2SO4ČÜŅŗµÄpH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
øł¾ŻŅŌĻĀ3øöČČ»Æѧ·½³ĢŹ½£ŗ
2H2S£Øg£©+3O2£Øg£©£½2SO2£Øg£©+2H2O£Øl£© ”÷H£½Q1 kJ/mol
2H2S£Øg£©+O2£Øg£©£½2S £Øs£©+2H2O£Øl£© ”÷H£½Q2 kJ/mol
2H2S£Øg£©+O2£Øg£©£½2S £Øs£©+2H2O£Øg£© ”÷H£½Q3 kJ/mol
ÅŠ¶ĻQ1”¢Q2”¢Q3ČżÕß¹ŲĻµÕżČ·µÄŹĒ
A£®Q1>Q2>Q3 B£®Q1>Q3>Q2 C£®Q3>Q2>Q1 D£®Q2>Q1>Q3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
2SO2£Øg£©+O2£Øg£©=2SO3£Øg£©·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾”£ŅŃÖŖ1mol SO2£Øg£©Ńõ»ÆĪŖ1mol SO3£Øg£©µÄ¦¤H= ”Ŗ99kJ”¤mol-1”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
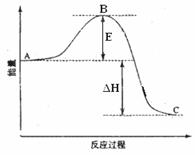
£Ø1£©Ķ¼ÖŠA±ķŹ¾ £¬EµÄ“󊔶ŌøĆ·“Ó¦µÄ·“Ó¦ČČ £ØĢī”°ÓŠ”±»ņ”°ĪŽ”±£©Ó°Ļģ”£øĆ·“Ó¦Ķس£ÓĆV2O5×÷“߻ƼĮ£¬¼ÓV2O5»įŹ¹Ķ¼ÖŠBµć £ØĢī”°Éżøß”±»¹ŹĒ”°½µµĶ”±£©£¬”÷H £ØĢī”°±ä“ó”±”¢”°±äŠ””±»ņ”°²»±ä”±£©£¬ĄķÓÉŹĒ ”£
£Ø2£©ŅŃÖŖµ„ÖŹĮņµÄČ¼ÉÕČČĪŖ296 KJ”¤mol-1£¬¼ĘĖćÓÉ S£Øs£©Éś³É3 molSO3£Øg£©µÄ”÷H£ØŅŖĒó¼ĘĖć¹ż³Ģ£©”£
S£Øs£©Éś³É3 molSO3£Øg£©µÄ”÷H£ØŅŖĒó¼ĘĖć¹ż³Ģ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÉčNA ĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( ””)
A£®1 L 0.1 mol•L£1µÄ°±Ė®ŗ¬ÓŠ0.1NAøöOH£
B£®1 L 1 mol”¤L£1µÄNaClOČÜŅŗÖŠŗ¬ÓŠClO£µÄŹżÄæĪŖNA
C£®25 ”ꏱ£¬pH =13µÄBa(OH)2ČÜŅŗÖŠŗ¬ÓŠOH£µÄŹżÄæĪŖ0 .1 NA
D£®ŌŚµē½ā¾«Į¶“ÖĶµÄ¹ż³ĢÖŠ£¬µ±Ņõ¼«Īö³ö32 gĶŹ±×ŖŅʵē×ÓŹżĪŖNA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«4.0 mol PCl3ŗĶ2.0 mol Cl2³äČėĢå»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśĻĀŹö·“Ó¦£ŗ PCl3(g)£«Cl2(g) PCl5(g)“ļµ½Ę½ŗāŹ±£¬PCl5ĪŖ0.80 mol£¬Čē¹ū“ĖŹ±ŅĘ×ß2.0 mol PCl3ŗĶ1.0 mol Cl2£¬ŌŚĻąĶ¬ĪĀ¶ČĻĀŌŁ“ļĘ½ŗāŹ±PCl5µÄĪļÖŹµÄĮæŹĒ ( ””)
PCl5(g)“ļµ½Ę½ŗāŹ±£¬PCl5ĪŖ0.80 mol£¬Čē¹ū“ĖŹ±ŅĘ×ß2.0 mol PCl3ŗĶ1.0 mol Cl2£¬ŌŚĻąĶ¬ĪĀ¶ČĻĀŌŁ“ļĘ½ŗāŹ±PCl5µÄĪļÖŹµÄĮæŹĒ ( ””)
A£®0.8 mol B£®0.4 mol C£®Š”ÓŚ0.4 mol D£®“óÓŚ0.4 mol£¬Š”ÓŚ0.8 mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
25 ”ꏱ£¬20.00 mLĮņĖįŗĶĻõĖįµÄ»ģŗĻČÜŅŗ£¬¼ÓČė×ćĮæµÄĀČ»Æ±µČÜŅŗ£¬³ä·Ö·“Ó¦ŗó¹żĀĖ”¢Ļ“µÓ”¢ŗęøÉ£¬æɵĆ0.466 g³Įµķ”£ĀĖŅŗøś2 mol/L NaOHČÜŅŗ·“Ó¦£¬ÓĆČ„10.00 mL¼īŅŗŹ±Ē”ŗĆÖŠŗĶ”£ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ( ””)
A£®Ō»ģŗĻŅŗÖŠc(SO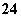 )£½0.2 mol/L B£®Ō»ģŗĻŅŗÖŠc(NO
)£½0.2 mol/L B£®Ō»ģŗĻŅŗÖŠc(NO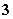 )£½0.9 mol/L
)£½0.9 mol/L
C£®Ō»ģŗĻŅŗÖŠpH£½0 D£®Ō»ģŗĻŅŗÖŠÓÉĖ®µēĄė³öµÄc(H£«)£½0.1 mol/L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½į¹¹¼ņŹ½ČēĶ¼µÄĶéĢž·Ö×ÓÖŠµÄŅ»øöĒāŌ×Ó±»ĀČŌ×ÓČ”“śŗó£¬æÉÄÜŠĪ³ÉµÄŅ»ĀČ“śĪļµÄÖÖĄąŹĒ(””””)

A£®1ÖÖ B£®2ÖÖ
C£®3ÖÖ D£®4ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĪļÖŹµÄĖ®ČÜŅŗ£¬ŅņĪŖĖ®½ā¶ųŹ¹ČÜŅŗ³ŹĖįŠŌµÄŹĒ
A£®NaHSO4 B£®NaHCO3 C£®AlCl3 D£®Na2SO4
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com