
| A. | 某元素从化合态变为游离态时,该元素一定被还原 | |
| B. | 含金属元素的离子一定是阳离子 | |
| C. | 金属单质只有还原性,金属阳离子不一定只有氧化性 | |
| D. | 不同的气体,若体积不同,则它们所含的分子数一定不同 |
分析 A.某元素从化合态变为游离态时,该元素不一定被还原,根据化合价的变化判断;
B.如AlO2-、MnO4-等,为阴离子;
C.当元素处于最低价态时只有还原性,当处于最高价态时只有氧化性,当处于中间价他时即有氧化性又有还原性;
D.气体的体积受温度、压强影响.
解答 解:A.某元素在化合态中可能显正价,也可能显负价,故当变为游离态时,该元素可能被还原,也可能被氧化,故A错误;
B.含金属元素的离子不一定是阳离子,如AlO2-、MnO4-等,为阴离子,故B错误;
C.当元素处于最低价态时只有还原性,当处于最高价态时只有氧化性,当处于中间价时即有氧化性又有还原性,金属单质处于元素的最低价态只有还原性,但金属阳离子不一定处于最高价态,如Fe2+,处于铁元素的中间价态,就即有氧化性又有还原性,故C正确;
D.气体的体积受温度、压强影响,若都是1mol的气体,温度和压强不同时体积不同,但是它们所含的分子数相同,故D错误.
故选C.
点评 本题考查氧化还原反应、影响气体体积的因素,侧重于学生的分析能力的考查,注意从元素化合价的角度判断相关概念并认识相关物质的性质,难度不大,答题时注意能举出实例.


科目:高中化学 来源: 题型:选择题
| A. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增加 | |
| B. | 对于有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大 | |
| C. | 改变条件能使化学反应速率增大的主要原因是增大了反应物分子中活化分子的有效碰撞几率 | |
| D. | 对于本来不能发生的化学反应,改变条件可以使反应发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Na2O2和H2O 反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | 用氢氧化钠溶液除去金属铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| C. | 用食醋除去水瓶中的水垢:2CH3COOH+CO32-═2CH3COO-+CO2↑+H2O | |
| D. | 等体积、等浓度的Ba(OH)2浓溶液和NH4HCO3 浓溶液混合后并加热Ba2++OH-+HCO3-═BaCO3↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
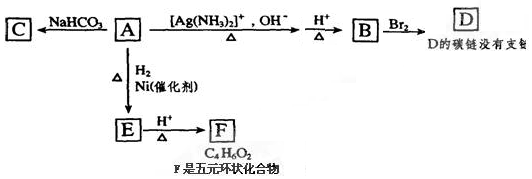
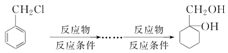
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2完全转化为SO3 | |
| B. | SO2、O2与SO3的物质的量之比为2:1:2 | |
| C. | 反应混合物中,SO3的质量分数不再改变 | |
| D. | 消耗2 mol SO2的同时生成2 mol SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
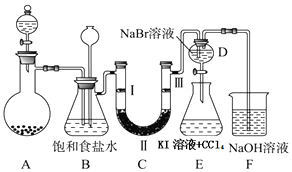
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 无水氯化钙 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 存在系统命名为1-甲基-2-乙基辛烷的烷烃,其分子式为C11H24 | |
| B. | 乙醛和丙烯醛(CH2=CHCHO)不是同系物,它们与氢气充分反应后的产物也不是同系物 | |
| C. | 通过测定反应前后溶液导电性的变化可判断在稀苯酚溶液中加入少量浓溴水时发生的是取代反应而不是加成反应 | |
| D. | 煤经加工所得的产物中存在大量的多环芳烃和稠环芳烃,如二甲联苯( )、萘( )、萘( )、蒽( )、蒽( )等,这些芳烃均属于苯的同系物 )等,这些芳烃均属于苯的同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com