

分析 A装置中反应制备CO2,其中有杂质HCl、H2O(g),B装置既减少CO2的溶解,又能吸收HCl,C装置干燥CO2,D装置制备碳酸氢钠,
(1)由图可知,A中生成二氧化碳,在D中二氧化碳与碳酸钠、水反应生成碳酸氢钠;
(2)B中酸可抑制二氧化碳的溶解;
(3)①Na2CO3和NaHCO3都能跟Ca(OH)2溶液发生反应生成白色沉淀;
②样液与BaCl2溶液混合,现白色沉淀并有气体产生,沉淀为碳酸钡、气体为二氧化碳;Na2CO3和BaCl2溶液混合也能生成沉淀;
③a.A点说明碳酸氢钠分解,残留率为63.09%;
b.B点残留率为80%,设原来有100克NaHCO3,反应后剩余80克,减少20克是CO2和H2O的质量,列方程组计算.
解答 解:A装置中反应制备CO2,其中有杂质HCl、H2O(g),B装置既减少CO2的溶解,又能吸收HCl,C装置干燥CO2,D装置制备碳酸氢钠,
(1)由图可知,A中生成二氧化碳,在D中二氧化碳与碳酸钠、水反应生成碳酸氢钠,该反应为Na2CO3+CO2+H2O═2NaHCO3,
故答案为:Na2CO3+CO2+H2O═2NaHCO3;
(2)B中酸可抑制二氧化碳的溶解,则B中溶液的作用为CO2在水中存在平衡:CO2+H2O?H2CO3?HCO3-+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体,
故答案为:CO2在水中存在平衡:CO2+H2O?H2CO3?HCO3-+H+,有H2SO4存在时,可使上述平衡向左移动,从而减少CO2在水中的溶解,同时吸收挥发出来的HCl气体;
(3)①Na2CO3和NaHCO3都能跟Ca(OH)2溶液发生反应生成白色沉淀,所以无法确定固体的成分中是否含有NaHCO3,
故答案为:Na2CO3和NaHCO3都能跟Ca(OH)2溶液发生反应生成白色沉淀,无法确定固体的成分中是否含有NaHCO3;
②样液与BaCl2溶液混合,现白色沉淀并有气体产生,沉淀为碳酸钡、气体为二氧化碳,离子反应为2HCO3-+Ba2+=BaCO3↓+CO2↑+H2O;Na2CO3和BaCl2溶液混合也能生成沉淀,则不能确定是否存在Na2CO3,结论合理,
故答案为:2HCO3-+Ba2+=BaCO3↓+CO2↑+H2O;合理;
③甲同学:取样液400mL,用pH计测溶液pH,再水浴加热蒸发至200mL,接下来的操作是冷却到室温,加水至溶液体积为400mL,再次测定pH,可确定固体存在碳酸氢钠,补充实验为取相同质量的纯净的NaHCO3配成1000mL溶液,取400mL,重复甲的实验,进行对照,
故答案为:冷却到室温,加水至溶液体积为400mL,再次测定pH;取相同质量的纯净的NaHCO3配成1000mL溶液,取400mL,重复甲的实验,进行对照;
乙同学:a.A点说明碳酸氢钠分解,残留率为63.09%,可知白色固体为碳酸氢钠,
故答案为:白色固体为NaHCO3;
b.B点残留率为80%,设原固体100g,则B点残留固体为80g,设生成碳酸钠为x,则
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O△m
106 62
x 100g-80g
则:x=$\frac{106(100g-80g)}{62}$=34.2g,
n(NaHCO3)=$\frac{80g-34.2g}{84g/mol}$=0.55mol,
n(Na2CO3)=$\frac{34.2g}{106g/mol}$=0.32mol,
n(NaHCO3):n(Na2CO3)=71:42,
故答案为:71:42.
点评 本题考查制备方案的设计,题目难度较大,涉及物质的性质、化学平衡、差量法计算、图象分析较等知识,试题知识点较多、综合性较强,(3)为解答的难点,试题培养了学生的分析能力及化学实验能力.


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯气是黄绿色气体,有毒,有刺激性气味,氯水还可杀菌消毒 | |
| B. | 液氯就是氯气的水溶液,它能使干燥的有色布条褪色 | |
| C. | 红热的铁丝在Cl2中燃烧产生棕色的雾;H2在Cl2中燃烧火焰呈淡蓝色 | |
| D. | 氯水长时间放置会变质,是因为氯气几乎完全挥发,剩下的就是水. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1×10-7 mol/L | B. | 1×10-12mol/L | C. | 1×10-2 mol/L | D. | 1×10-7 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.24L | B. | 3.36L | C. | 1.12L | D. | 4.48L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鱼虾放久了会产生不愉快的腥臭气味,应当用水冲洗,并在烹调时加人少量食醋 | |
| B. | “酸可除锈”“洗涤剂可去油”都是发生了化学变化 | |
| C. | 被蜂蚁蜇咬会感到疼痛难忍,这是蜂蚁咬人时将甲酸注人人体的缘故,此时若能涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛 | |
| D. | 煤酚皂溶液可用于环境消毒,医用酒精可用于皮肤消毒,其原因均在于可以使蛋白质发生变性凝固 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
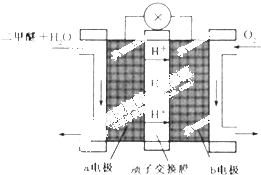 二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
二甲醚(CH3OCH3)被称为21世界的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0L 0.1mol•L-1戊溶液中阴离子总的物质的量大于0.1mol | |
| B. | 将足量甲加入到酚酞试液中,溶液先变红后褪色 | |
| C. | X与W构成的化合物、戊、己均为离子化合物 | |
| D. | W的简单离子半径大于Z的简单离子半径 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
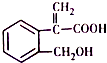
| A. | 分子式为C10H10O3 | |
| B. | 1mol 该有机物最多可与5mol氢气发生加成反应 | |
| C. | 该有机物在一定条件下,可以发生取代、氧化、消去反应 | |
| D. | 1mol 该有机物与足量钠反应生成22.4L氢气(标况下) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com