
【题目】下列说法正确的是
A. 0.2 mol·L-1与0.1 mol·L-1 HClO溶液中c(H+)之比为2:1
B. pH=2和pH=1的硝酸中c(H+)之比为1:2
C. 25 ℃时,0.1 mol·L-1CH3COOH的电离平衡常数K=2×10-5,则0.1 mol·L-1CH3COONa的水解平衡常数为5×10-10
D. 0.1 mol·L-1NaHCO3溶液中:c (Na+)+ c (H+)+ c (H2CO3)<c (HCO3-) +3 c (CO32-) + c (OH-)
【答案】C
【解析】A、HClO是弱电解质,溶液越稀,电离程度越大,故0.2mol/L的HClO溶液中的氢离子浓度小于0.1mol/LHClO溶液中的氢离子浓度的2倍,即两溶液中的c(H+)之比小于2:1,故A错误;B、c(H+)=10-pH,故pH=2的硝酸溶液中,c(H+)=0.01mol/L;而pH=1的硝酸溶液中,c(H+)=0.1mol/L,故两溶液中的c(H+)之比为1:10,故B错误;C. 25 ℃时,0.1 mol·L-1CH3COOH的电离平衡常数K=2×10-5,则0.1 mol·L-1CH3COONa的水解平衡常数=![]() =
=![]() =5×10-10,故C正确;D. 0.1 mol·L-1NaHCO3溶液中存在电荷守恒,c (Na+)+ c (H+)= c (HCO3-) +2c (CO32-) + c (OH-),因为水解程度大于电离程度,因此c (H2CO3)> c (CO32-),则c (Na+)+ c (H+)+ c (H2CO3)>c (HCO3-) +3 c (CO32-) + c (OH-),故D错误;故选C。
=5×10-10,故C正确;D. 0.1 mol·L-1NaHCO3溶液中存在电荷守恒,c (Na+)+ c (H+)= c (HCO3-) +2c (CO32-) + c (OH-),因为水解程度大于电离程度,因此c (H2CO3)> c (CO32-),则c (Na+)+ c (H+)+ c (H2CO3)>c (HCO3-) +3 c (CO32-) + c (OH-),故D错误;故选C。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.酸性氧化物都不能与酸发生反应
B.氯水中的次氯酸具有杀菌消毒的作用
C.铵盐受热分解都能放出氨气
D.生物固氮是指植物通过叶面直接吸收空气中的氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【加试题】以氧化铝为原料,通过碳热还原法可合成氮化铝(AlN);通过电解法可制取铝。电解铝时阳极产生的CO2可通过二氧化碳甲烷化再利用。请回答:
(1)已知:2Al2O3(s)===4Al(g)+3O2(g) ΔH1=3351 kJ·molˉ1
2C(s)+O2(g)===2CO(g) ΔH2=-221 kJ·molˉ1
2Al(g)+N2(g)===2AlN(s) ΔH3=-318 kJ·molˉ1
碳热还原Al2O3合成AlN的总热化学方程式是 , 该反应自发进行的条件 。
(2)在常压、Ru/TiO2催化下,CO2和H2混和气体(体积比1∶4,总物质的量a mol)进行反应,测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)。
反应Ⅰ CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g) ΔH4
CH4(g)+2H2O(g) ΔH4
反应Ⅱ CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH5
CO(g)+H2O(g) ΔH5
①下列说法不正确的是
A.ΔH 4小于零
B.温度可影响产物的选择性
C.CO2平衡转化率随温度升高先增大后减少
D.其他条件不变,将CO2和H2的初始体积比改变为1∶3,可提高CO2平衡转化率
②350℃时,反应Ⅰ在t1时刻达到平衡,平衡时容器体积为V L,该温度下反应Ⅰ的平衡常数为(用a、V表示)
(3)350℃下CH4物质的量随时间的变化曲线如图3所示。画出400℃下0~t1时刻CH4物质的量随时间的变化曲线。
(4)据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B3C+5D反应中,表示该反应速率最快的是( )
A.v(A)═0.5 mol/(Ls)
B.v(B)═0.3mol/(Ls)
C.v(C)═0.8 mol/(Ls)
D.v(D)═1mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中可以大量共存,加OH﹣产生沉淀,加H+生成气体的一组离子是( )
A.Na+、Cu2+、CO ![]() 、Cl﹣
、Cl﹣
B.Na+、Cl﹣、HCO ![]() 、Mg2+
、Mg2+
C.Cl﹣、NO ![]() 、K+、Ca2+
、K+、Ca2+
D.NH ![]() 、K+、H+、SO
、K+、H+、SO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,A处通入Cl2 , 关闭B阀时,C处的红布看不到明显现象;当打开B阀后,C处红布条逐渐褪色.则D瓶中装的是( ) 
A.浓盐酸
B.NaOH溶液
C.H2O
D.饱和NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机非金属材料.为了分析某AlN样品(样品中的杂质不与氢氧化钠溶液反应)中A1N的含量,某实验小组设计了如下两种实验方案.
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案l】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去).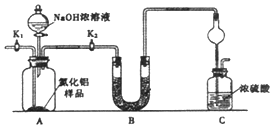
(1)如图C装置中球形干燥管的作用是 .
(2)完成以下实验步骤:组装好实验装置后,首先 ,
再加入实验药品.接下来关闭K1 , 打开K2 , 打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体.打开K1 , 通入氮气一段时间,测定C装置反应前后的质量变化.通入氮气的目的是 .
(3)装置B中试剂可以为(选正确序号填空).
①浓硫酸 ②碱石灰 ③P2O5④还原铁粉
若去掉装置B,则导致测定结果 (填“偏高”、“偏低”或“无影响”).由于上述装置还存在缺陷,导致测定结果偏高,请提出改进意见 .
(4)【方案2】按以下步骤测定样品中A1N的纯度: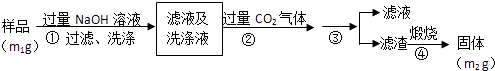
步骤②生成沉淀的离子方程式为 .
步骤③的操作是 . A1N的纯度是 (用m1、m2表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的离子方程式或化学方程式.
(1)用稀硫酸清除铁锈(Fe2O3)(写出离子方程式):
(2)FeCl3溶液中加入NaOH溶液(写出离子方程式):
(3)盐酸跟碳酸氢钠溶液反应(写出离子方程式):
(4)少量CO2通入澄清石灰水中(写出离子方程式): .
(5)Cu2++2OH﹣=Cu(OH)2↓(写出化学方程式) .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com