
£Ø15·Ö£©Ä³Š”×éĶ¬Ń§ĄūÓĆĀĮŗĶŃõ»ÆĢś·¢ÉśĀĮČČ·“Ó¦ŗóµĆµ½µÄ¹ĢĢå½ųŠŠČēĻĀŹµŃ锣
£Ø1£©ĀĮŗĶŃõ»ÆĢś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ ”£
£Ø2£©¹ĢĢå³É·ÖµÄ³õ²½Č·¶Ø”£
ŹµŃéŠņŗÅ | ²Ł×÷¼°ĻÖĻó |
¢” | ȔɣĮæ¹ĢĢåѳʷ£¬¼ÓČė¹żĮæĻ”ŃĪĖį£¬¹ĢĢåČܽā£¬²śÉśĪŽÉ«ĘųĢå£Ø¾¼ģŃéĪŖH2£©£¬ČÜŅŗ³ŹĒ³»ĘÉ« |
¢¢ | Ļņ¢”ÖŠĖłµĆČÜŅŗÖŠ¼ÓČėÉŁĮæKSCNČÜŅŗ£¬ČÜŅŗ³ŹĒ³ŗģÉ«£¬ŌŁ¼ÓČėH2O2ČÜŅŗÖĮ¹żĮ棬²śÉśĪŽÉ«ĘųĢå£Ø¾¼ģŃéĪŖO2£©£¬ČÜŅŗ±äĪŖÉīŗģÉ«£¬ĒŅŗģÉ«ŗÜæģĶŹČ„ |
¢ŁÓÉÉĻŹöŹµŃéæÉÖŖ£ŗČÜŅŗÖŠFeŌŖĖŲµÄ“ęŌŚŠĪŹ½ÓŠ ”£
¢Ś¢”ÖŠ²śÉśH2µÄŌŅņŹĒѳʷ֊³żŗ¬FeĶā£¬æÉÄÜÓŠĪ“·“Ó¦µÄAl£¬ĪŖ¼ģŃéѳʷ֊ŹĒ·ńŗ¬Alµ„ÖŹ£¬Éč¼ĘĮĖĻą¹ŲŹµŃ飬ŅĄ¾ŻµÄŌĄķŹĒ£ØÓĆĄė×Ó·½³ĢŹ½±ķŹ¾£© ”£
¢ŪÉś³ÉO2µÄ»Æѧ·½³ĢŹ½ŹĒ ”£
½ųŅ»²½µÄŹµŃé±ķĆ÷£¬ÉĻŹö¹ĢĢåѳʷ֊FeŌŖĖŲµÄ“ęŌŚŠĪŹ½ÓŠ£ŗFe”¢Fe2O3”¢Fe3O4”£
£Ø3£©øĆŠ”×éĶ¬Ń§¶Ō¢¢ÖŠČÜŅŗŗģÉ«ĶŹČ„µÄŌŅņ×ö½ųŅ»²½Ģ½¾æ”£
ŹµŃéŠņŗÅ | ²Ł×÷”¢ĻÖĻó |
¢£ | ½«¢¢ÖŠŹ£ÓąČÜŅŗ¾ł·ÖĪŖĮ½·Ż£¬Ņ»·ŻµĪ¼ÓNaOHČÜŅŗ£¬²śÉśŗģŗÖÉ«³Įµķ£» ĮķŅ»·ŻµĪ¼ÓBaCl2ČÜŅŗ£¬²śÉś°×É«³Įµķ£¬¼ÓČėŃĪĖį£¬³Įµķ²»Čܽā |
¢¤ | Č”2 mL 0.1 mol/L FeCl3ČÜŅŗ£¬µĪČėKSCNČÜŅŗ£¬ČÜŅŗ±äĪŖŗģÉ«£¬ĶØČėŅ»¶ĪŹ±¼äO2£¬ĪŽĆ÷ĻŌ±ä»Æ”£ŌŁ¼ÓČėH2O2ČÜŅŗ£¬ŗģÉ«ŗÜæģĶŹČ„ |
ĢįŹ¾£ŗKSCNÖŠSŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ-2¼Ū
¢ŁŹµŃ颣֊°×É«³ĮµķµÄ»ÆѧŹ½ŹĒ ”£
¢Ś½įŗĻŹµŃ颣ŗĶ¢¤·ÖĪö£¬ŹµŃ颢֊ŗģÉ«ĶŹČ„µÄŌŅņŹĒ ”£
¢Ū²éŌÄ׏ĮĻµĆÖŖ£ŗCl-¶ŌČÜŅŗŗģÉ«ĶŹČ„µÄ·“Ó¦ÓŠ“ß»Æ×÷ÓĆ£¬ŃéÖ¤øĆĖµ·ØÓ¦²¹³äµÄŹµŃéŗĶĻÖĻóŹĒ ”£

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ŌĘÄĻŹ”øßŅ»3ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠø÷×éĪļÖŹÖŠ£¬ĄØŗÅÄŚĪŖŌÓÖŹ£¬ĘäÖŠ³żŌÓ·½·Ø²»ÕżČ·µÄŹĒ
A£®Na2CO3¹ĢĢå£ØNaHCO3£© ¼ÓČČ B£®I2£ØÉ°×Ó£© ¼ÓČČ
C£®Na2O2£ØNa2O£© ŃõĘųÖŠ¼ÓČČ D£®Cl2£ØHCl£© ĶعżNaOHČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ±±¾©ŹŠŗ£µķĒųøßČżŅ»Ä£Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ½āŹĶŹĀŹµµÄ·½³ĢŹ½ÕżČ·µÄŹĒ
A£®ŌŚæÕĘųÖŠĒŠæŖ½šŹōÄĘ£¬¹āĮĮ±ķĆę±ä°µ£ŗ2Na£«O2===Na2O2
B£®ĻņĀČ»ÆĀĮČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£¬²śÉś°×É«³Įµķ£ŗAl3+ + 3OH-===Al(OH)3”ż
C£®½«Ģś·ŪÓėĖ®ÕōĘų¹²ČČ£¬²śÉśĘųĢå£ŗ2Fe£«3H2O(g)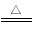 Fe2O3£«3H2
Fe2O3£«3H2
D£®µē½ā±„ŗĶĀČ»ÆÄĘČÜŅŗ£¬²śÉśĘųĢå£ŗ2NaCl+2H2O  2NaOH£«H2”ü£«Cl2”ü
2NaOH£«H2”ü£«Cl2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğøŹĖąŹ”ĢģĖ®ŹŠøßČżĻĀѧʌ¶žÄ£æ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
”²»Æѧ”ŖŃ”ŠŽ3£ŗĪļÖŹ½į¹¹ÓėŠŌÖŹ”³(15·Ö)ŅŃÖŖA”¢B”¢C”¢D”¢EĪåÖÖŌŖĖŲµÄŌ×ÓŠņŹżŅĄ“ĪµŻŌö£¬A”¢B”¢C”¢DĪ»ÓŚ¶ĢÖÜĘŚ”£AĪ»ÓŚÖÜĘŚ±ķµÄsĒų£¬ĘäŌ×ÓÖŠµē×Ó²ćŹżŗĶĪ“³É¶Ōµē×ÓŹżĻąĶ¬£»BµÄ»łĢ¬Ō×ÓÖŠµē×ÓÕ¼¾ŻČżÖÖÄÜĮæ²»Ķ¬µÄŌ×Ó¹ģµĄ£¬ĒŅĆæÖÖ¹ģµĄÖŠµÄµē×Ó×ÜŹżĻąĶ¬£»DŌ×Ó×īĶā²ćµē×ÓŹżŹĒ“ĪĶā²ćµē×ÓŹżµÄ3±¶”£EÓŠ”°ÉśĪļ½šŹō”±Ö®³Ę£¬E4£«ŗĶė²Ō×ÓµÄŗĖĶāµē×ÓÅŲ¼ĻąĶ¬”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©B”¢C”¢DČżÖÖŌŖĖŲµÄµēøŗŠŌÓÉŠ”µ½“óµÄĖ³ŠņĪŖ £¬EµÄ»łĢ¬Ō×ӵĵē×ÓÅŲ¼Ź½ĪŖ ”£
£Ø2£©ÓÉB”¢DŠĪ³ÉµÄBD32 £Ąė×ÓÖŠ£¬ĘäVSEPRÄ£ŠĶĆū³ĘŹĒ £¬Ąė×ÓµÄÖŠŠÄŌ×Ó²ÉÓĆ ŌӻƔ£
£Ø3£©ŅŃÖŖÓÉA”¢C”¢DČżÖÖŌŖĖŲ°“ÕÕ4:2:3µÄŌ×ÓøöŹż±ČæÉŠĪ³ÉijĄė×Ó»ÆŗĻĪļ£¬³£ĪĀĻĀ²āµĆøĆĄė×Ó»ÆŗĻĪļµÄĖ®ČÜŅŗpH=5£¬ŌņøĆČÜŅŗÖŠĖ®µēĄė³öµÄĒāĄė×ÓÅضČĪŖ ”£
£Ø4£©D”¢EŗĶ±µČżÖÖŌŖĖŲ¹¹³ÉµÄij»ÆŗĻĪļµÄ¾§°ū½į¹¹ČēĶ¼ĖłŹ¾£¬øĆ»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖ ”£

ÄÉĆ×¼¶µÄEO2ŹĒŅ»ÖÖ¹ć·ŗŹ¹ÓĆµÄ“ß»Æ¼Į£¬ŹµŃéŹŅĶłĶłĶعżECl4ŌŚ“óĮæĖ®ÖŠ¼ÓČČĖ®½āÖʵĆEO2”¤xH2O£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğøŹĖąŹ”ĢģĖ®ŹŠøßČżĻĀѧʌ¶žÄ£æ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ā±ĖŲ»„»ÆĪļÓėĀ±ĖŲµ„ÖŹŠŌÖŹĻąĖĘ”£ŅŃÖŖCH2£½CH”ŖCH£½CH2(1£¬3”Ŗ¶”¶žĻ©)ÓėĀČĘų·¢Éś¼Ó³É²śĪļÓŠČżÖÖ£ŗ
¢ŁCH2Cl”ŖCHCl”ŖCH£½CH2 (1£¬2”Ŗ¼Ó³É)
¢ŚCH2Cl”ŖCH£½CH”ŖCH2Cl (1£¬4”Ŗ¼Ó³É)
¢ŪCH2Cl”ŖCHCl”ŖCHCl”ŖCH2Cl(ĶźČ«¼Ó³É)
¾Ż“ĖĶĘ²āCH2£½C(CH3)”ŖCH£½CH2(ŅģĪģ¶žĻ©)ÓėĀ±ĖŲ»„»ÆĪļBrClµÄ¼Ó³É²śĪļÓŠ¼øÖÖ(²»æ¼ĀĒĖ³·“Ņģ¹¹ŗĶ¾µĻńŅģ¹¹
A£®6ÖÖ B£®10ÖÖ C£®12ÖÖ D£®14ÖÖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ±±¾©ŹŠĪ÷³ĒĒųøßČż¶žÄ£Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅĄ¾ŻĻĀĮŠŹµŃéĻÖĻó£¬µĆ³öµÄ½įĀŪÕżČ·µÄŹĒ
²Ł×÷ | ŹµŃéĻÖĻó | ½įĀŪ | |
A | ĻņNaBrČÜŅŗÖŠ¼ÓČėĀČĖ®£¬ŌŁ¼ÓČėµķ·ŪKIČÜŅŗ | ČÜŅŗ±äĄ¶ | Ńõ»ÆŠŌ£ŗCl2>Br2>I2 |
B | ½«ĀĮʬ·ÅČėŃĪĖįÖŠ | ²śÉśĘųÅŻµÄĖŁĀŹæŖŹ¼Ź±½ĻĀż£¬Ėęŗó¼Óæģ£¬ŗóĄ“ÓÖÖš½„¼õĀż | H+µÄÅØ¶ČŹĒÓ°Ļģ·“Ó¦ĖŁĀŹµÄĪØŅ»ŅņĖŲ |
C | ĻņÕįĢĒČÜŅŗÖŠ¼ÓČėĻ”ĮņĖį£¬Ė®Ō”¼ÓČČŗ󣬼ÓČėŠĀÖĘĒāŃõ»ÆĶ£¬¼ÓČČ | µĆµ½Ą¶É«ČÜŅŗ | ÕįĢĒĖ®½ā²śĪļƻӊ»¹ŌŠŌ |
D | ĻņĘÆ°×·ŪÖŠµĪČėÅØŃĪĖį£¬½«Éś³ÉµÄĘųĢåĶØČėĘ·ŗģČÜŅŗ | Ę·ŗģČÜŅŗĶŹÉ« | ĘųĢåÖŠŗ¬ÓŠCl2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ±±¾©ŹŠŗ£µķĒųøßČżµŚ¶žŃ§ĘŚĘŚÄ©Į·Ļ°Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ¼ņ“šĢā
£Ø14·Ö£©Ä³ÖÖļ®Ąė×Óµē³ŲµÄÕż¼«²ÄĮĻŹĒ½«ŗ¬ÓŠīÜĖįļ®£ØLiCoO2£©µÄÕż¼«·Ū¾łŌČĶæø²ŌŚĀĮ²ÉĻÖĘ³ÉµÄ£¬æÉŅŌŌŁÉśĄūÓĆ”£Ä³Š£ŃŠ¾æŠ”×é³¢ŹŌ»ŲŹÕ·Ļ¾ÉÕż¼«²ÄĮĻÖŠµÄīÜ”£
£Ø1£©25”ꏱ£¬ÓĆĶ¼1ĖłŹ¾×°ÖĆ½ųŠŠµē½ā£¬ÓŠŅ»¶ØĮæµÄīÜŅŌCo2+µÄŠĪŹ½“ÓÕż¼«·ŪÖŠ½ž³ö£¬ĒŅĮ½¼«¾łÓŠĘųÅŻ²śÉś£¬Ņ»¶ĪŹ±¼äŗóÕż¼«·ŪÓėĀĮ²°žĄė”£
¢ŁŅõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗLiCoO2 + 4H+ + e- === Li+ + Co2+ + 2H2O ”¢ ”£
Ńō¼«µÄµē¼«·“Ó¦Ź½ĪŖ ”£
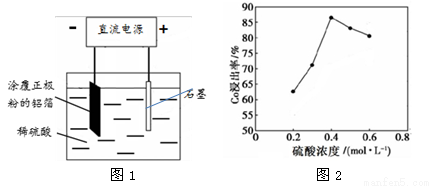
¢ŚøĆŃŠ¾æŠ”×é·¢ĻÖĮņĖįÅØ¶Č¶ŌīܵĽž³öĀŹÓŠ½Ļ“óÓ°Ļģ£¬Ņ»¶ØĢõ¼žĻĀ£¬²āµĆĘä±ä»ÆĒśĻßČēĶ¼2ĖłŹ¾”£µ±c(H2SO4) > 0.4 mol”¤L-1Ź±£¬īܵĽž³öĀŹĻĀ½µ£¬ĘäŌŅņæÉÄÜĪŖ ”£
£Ø2£©µē½āĶź³ÉŗóµĆµ½ŗ¬Co2+µÄ½ž³öŅŗ£¬ĒŅÓŠÉŁĮæÕż¼«·Ū³Į»żŌŚµē½ā²Ūµ×²æ”£ÓĆŅŌĻĀ²½Öč¼ĢŠų»ŲŹÕīÜ”£
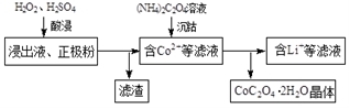
¢ŁŠ“³ö”°Ėį½ž”±¹ż³ĢÖŠÕż¼«·Ū·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£øĆ²½ÖčŅ»°ćŌŚ80”ęŅŌĻĀ½ųŠŠ£¬ĪĀ¶Č²»ÄÜĢ«øßµÄŌŅņŹĒ ”£
¢ŚŅŃÖŖ(NH4)2C2O4ČÜŅŗ³ŹČõĖįŠŌ£¬ĻĀĮŠ¹ŲĻµÖŠÕżČ·µÄŹĒ £ØĢī×ÖÄøŠņŗÅ£©”£
a.c (NH4+)> c(C2O42-)>c (H+)>c (OH-)
b.c (H+) +c (NH4+) =c (OH-) + c(HC2O4-)+c(C2O42-)
c.c (NH4+)+ c (NH3H2O ) = 2[c(C2O42-) + c(HC2O4-) + c(H2C2O4)]
£Ø3£©ŅŃÖŖĖłÓĆļ®Ąė×Óµē³ŲµÄÕż¼«²ÄĮĻĪŖx g£¬ĘäÖŠLiCoO2£ØM = 98 g”¤mol-1£©µÄÖŹĮæ·ÖŹżĪŖa%£¬Ōņ»ŲŹÕŗóµĆµ½CoC2O42H2O £ØM = 183 g”¤mol-1£©µÄÖŹĮæ²»øßÓŚ g”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğ±±¾©ŹŠŗ£µķĒųøßČż4ŌĀÄ£ÄāĮ·Ļ°»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃé²Ł×÷ÖŠÓŠ“ķĪóµÄŹĒ
A£®·ÖŅŗŹ±,·ÖŅŗĀ©¶·ĻĀ²ćŅŗĢå“ÓĻĀæŚ·Å³ö,ÉĻ²ćŅŗĢå“ÓÉĻæŚµ¹³ö
B£®ÕōĮó²Ł×÷Ź±,Ó¦Ź¹ĪĀ¶Č¼ĘĖ®ŅųĒņææ½üÕōĮóÉÕĘæµÄÖ§¹ÜæŚ“¦
C£®ÕōĮóÖŠ,ĄäČ“Ė®Ó¦“ÓĄäÄż¹ÜµÄĻĀæŚĶØČė,ÉĻæŚĮ÷³ö
D£®Õō·¢²Ł×÷Ź±,Ó¦Ź¹»ģŗĻĪļÖŠµÄĖ®·ÖĶźČ«ÕōøÉŗó,ŌŁĶ£Ö¹¼ÓČČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014-2015ѧğÉĻŗ£ŹŠĪ劣øßČżµŚ¶žŃ§ĘŚĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚøÜøĖµÄĮ½¶Ė·Ö±š¹Ņ×ÅÖŹĮæŗĶĢå»ż¶¼ĻąĶ¬µÄĀĮĒņŗĶĢśĒņ£¬“ĖŹ±øÜøĖĘ½ŗā”£Č»ŗó½«Į½Ēņ·Ö±š½žĆ»ŌŚĒāŃõ»ÆÄĘČÜŅŗŗĶĮņĖįĶČÜŅŗ֊ʬæĢ(ČēĻĀĶ¼ĖłŹ¾)£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
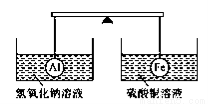
A£®Į½ÉÕ±ÖŠ¾łĪŽĘųÅŻ²śÉś B£®×ó±ßÉÕ±ÖŠµÄČÜŅŗÖŹĮæ¼õÉŁĮĖ
C£®Č„µōĮ½ÉÕ±£¬øÜøĖČŌĘ½ŗā D£®ÓŅ±ßĢśĒņÉĻ³öĻÖŗģÉ«
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com