
实验发现,298K时,在FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+。某化学兴趣小组根据该实验事实设计了如下图所示的原电池装置。下列有关说法中正确的是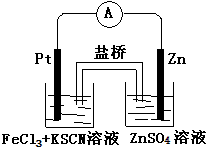

科目:高中化学 来源: 题型:
 (2012?吉林一模)实验发现,298K时,在FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+.某化学兴趣小组根据该实验事实设计了如图所示的原电池装置.下列有关说法中正确的是( )
(2012?吉林一模)实验发现,298K时,在FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+.某化学兴趣小组根据该实验事实设计了如图所示的原电池装置.下列有关说法中正确的是( )查看答案和解析>>
科目:高中化学 来源:2011-2012学年吉林省吉林市高三上学期期末考试化学试卷 题型:选择题
实验发现,298K时,在FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+。某化学兴趣小组根据该实验事实设计了如下图所示的原电池装置。下列有关说法中正确的是
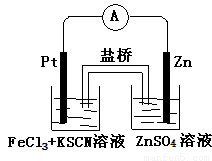
A.该原电池的正极反应是:Zn—2e-=Zn2+
B.左烧杯中溶液的红色逐渐褪去
 C.该电池铂电极上有气泡出现
C.该电池铂电极上有气泡出现
D.该电池总反应为:3Zn + 2Fe3+ = 2Fe + 3Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
(7分)实验发现,298K时,在FeCl3的酸性溶液中通入氢气,Fe3+被还原成Fe2+离子的反应并不能发生,但在FeCl3酸性溶液中加少量锌粒后反应该立即进行。有人用“新生态”概念解释此实验现象,认为锌与酸作用时产生的“新生态”氢原子H*来不及结合成H2即与FeCl3作用,反应式为:Zn+2H+![]() 2H*+Zn2+,H*+FeCl3
2H*+Zn2+,H*+FeCl3![]() FeCl2+HCl。但这种解释争议颇多。有化学工作者指出,根据298K时两电对的标准电极电势E$(Zn2+/Zn)=-0.763V,
FeCl2+HCl。但这种解释争议颇多。有化学工作者指出,根据298K时两电对的标准电极电势E$(Zn2+/Zn)=-0.763V,
E$ (Fe3+/Fe2+)=0.771V和设计下述原电池实验即可判断上述解释正确与否:
在两只烧杯中分别装入ZnSO4和FeCl3溶液,再在ZnSO4中插入锌片,在FeCl3中插入铂片,并加数滴KSCN使溶液呈红色,将两极用盐桥连接后,装有FeCl3溶液的烧杯中的红色逐渐褪去。如果在FeCl3溶液内加少量酸,褪色更快。请回答下列问题:
(1) 所设计的原电池符号是 ;
(2) 该原电池的正极反应是 ;
负极反应是 ;
原电池的总反应是 。
(3) 上述关于“新生态”H*的解释是否正确 (填“是”或“否”),理由是:
。
(4) 说明加酸后褪色更快的原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验发现,298K时,在FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+。某化学兴趣小组根据该实验事实设计了如下图所示的原电池装置。下列有关说法中正确的是
A.该原电池的正极反应是:Zn—2e-=Zn2+
B.左烧杯中溶液的红色逐渐褪去
![]() C.该电池铂电极上有气泡出现
C.该电池铂电极上有气泡出现
D.该电池总反应为:3Zn + 2Fe3+ = 2Fe + 3Zn2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com