


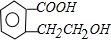 ,A和HBr发生取代反应生成C,C发生反应生成D,D和溴发生加成反应,则C发生消去反应生成D,D的结构简式为
,A和HBr发生取代反应生成C,C发生反应生成D,D和溴发生加成反应,则C发生消去反应生成D,D的结构简式为 ,E发生消去反应和酯化反应生成F,再结合题目分析解答.
,E发生消去反应和酯化反应生成F,再结合题目分析解答.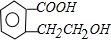 ,A和HBr发生取代反应生成C,C发生反应生成D,D和溴发生加成反应,则C发生消去反应生成D,D的结构简式为
,A和HBr发生取代反应生成C,C发生反应生成D,D和溴发生加成反应,则C发生消去反应生成D,D的结构简式为 ,E发生消去反应和酯化反应生成F,
,E发生消去反应和酯化反应生成F,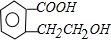 ,则A中官能团为羧基和羟基,根据结构简式知A的分子式为C9H10O3,
,则A中官能团为羧基和羟基,根据结构简式知A的分子式为C9H10O3, ,
, ;
;
 .
.


科目:高中化学 来源: 题型:

| A、绿原酸能使酸性KMnO4溶液褪色 |
| B、绿原酸水解产物均可以与FeCl3溶液发生显色反应 |
| C、1mol绿原酸与足量溴水反应,最多消耗2.5mol Br2 |
| D、1mol绿原酸与足量NaOH溶液反应,最多消耗8mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ?mol-1,则氢气的燃烧热为241.8 kJ?mol-1 |
| B、已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3 kJ?mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量 |
| C、已知2C(s)+2O2(g)═2CO2(g)△H=a;2C(s)+O2(g)═2CO(g)△H=b,则a>b |
| D、已知C(石墨,s)═C(金刚石,s)△H>0,则石墨比金刚石稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 定量测定化学反应速率 |
B、 验证Na和水反应的热效应 |
C、 比较KMnO4、Cl2、S的氧化性 |
D、 加热烧杯,分离SiO2和NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸 | 电离方程式 | 电离常数 K/mol?L-1 |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.26×10-5 |
| H2CO3 | H2CO3?H++HCO3- HCO3-?CO32-+H+ | K1=4.31×10-7 K2=5.61×10-11 |
| H2S | H2S?H++HS- HS-?H++S2- | K1=9.1×10-8 K2=1.1×10-12 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com