
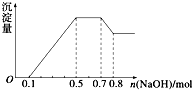
 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )| A、溶液中的阳离子有H+、Mg2+、NH4+、Al3+ |
| B、溶液中n (Al3+)=0.2mol |
| C、溶液中一定不含CO32-,可能含有SO42-和NO3- |
| D、n(H+):n(Al3+):n(Mg2+)=2:2:1 |


科目:高中化学 来源: 题型:
| A、反应①中Se是氧化产物,I2是还原产物 |
| B、反应②中浓H2SO4是氧化剂,SeO2是还原产物 |
| C、反应①中每有1.0mol I2生成,转移电子数目为4NA |
| D、SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)>SeO2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | X | Y | Z | W |
| 初始浓度/mol?L-1 | 0.5 | 0.6 | 0 | 0 |
| 平衡浓度/mol?L-1 | 0.1 | 0.1 | 0.4 | 0.6 |
| A、反应达到平衡时,X的转化率为80% | ||
B、该反应的平衡常数表达式为K=
| ||
| C、增大压强其平衡常数不变,但使平衡向生成Z的方向移动 | ||
| D、改变温度可以改变此反应的平衡常数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ①KMnO4、OH- | ||
|
| HBr |
| 过氧化物 |
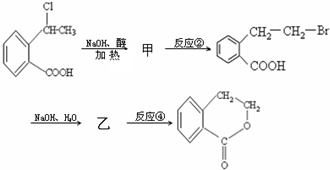
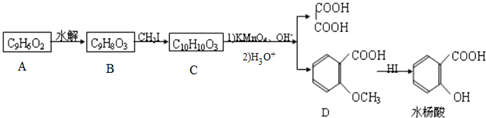
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用FeCl3溶液腐蚀印刷电路板:2Fe3++Cu═2Fe2++Cu2+ |
| B、氢氧化钡溶液跟硫酸反应:OH-+H+═H2O |
| C、碳酸钙与盐酸反应:2H++CO32-=H2O+CO2↑ |
| D、氧化铜与稀硫酸混合:CuO+H+═Cu2++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
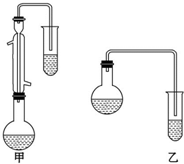 某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |

查看答案和解析>>
科目:高中化学 来源: 题型:
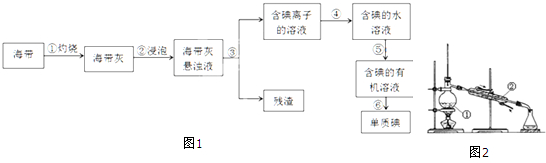
查看答案和解析>>
科目:高中化学 来源: 题型:
A、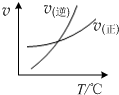 表示的反应速率随温度变化的关系可知该反应的△H>0 |
B、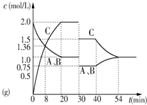 代表等物质的量的气体A和B,在一定温度下发生反应A(g)+B(g)?2C(g),达到平衡后,只改变反应的一个条件,其在20~40 min之间的平衡常数不相等 |
C、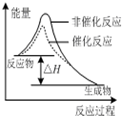 表示该反应为放热反应,且催化剂不能改变反应的焓变 |
D、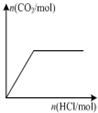 表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com