
����Ҫ0.1mol/L��NaOH��Һ480mL��ʵ�����ù����ռ������ƣ���ش�
��1�������ȡ��NaOH����������� g��
��2�����������������ձ� ��ҩ�� ��250mL����ƿ ��500mL����ƿ �ݲ����� ��������ƽ ����Ͳ������ʱ������ʹ�õIJ��������� ������ţ�����ȱ�ٵIJ��������� ��
��3��ʹ������ƿǰ������е�һ�������� ��
��4��������Һʱ���ڼ��㡢�������ܽ⡢��ȴ�������¼������裬����ȷ�IJ���˳��Ϊ_ ������ţ�������ҡ�ȣ���ϴ�ӣ��۶��ݣ��ܵߵ�ҡ�ȣ���ת�ơ�
��5�����ƹ����У����в�����������ƫ�ߵ��� ������ţ���
��δϴ���ձ�����������
�ڳ���NaOH��ʱ��̫����
�۶���ʱ���ӿ̶ȣ�
��NaOH��Һδ��ȴ�����¾�ת�Ƶ�����ƿ�С�
��6���ֽ�200mL0.01mol/LNaOH��50mL0.02mol/LCa(OH)2��Һ��ϣ���Ϻ�����仯���Բ��ƣ���������Һ��OH�������ʵ���Ũ���� mol/L��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������տ�����ѧ�߶���12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��Ӧ��A(g)+3B(g) 2C(g) [��H��0]��ƽ�������������¶Ƚ��ͣ�������������ȷ���ǣ� ��
2C(g) [��H��0]��ƽ�������������¶Ƚ��ͣ�������������ȷ���ǣ� ��
A������Ӧ���ʼӴ��淴Ӧ���ʱ�С��ƽ��������Ӧ�����ƶ�
B������Ӧ���ʼ�С���淴Ӧ���ʼӴ�ƽ�����淴Ӧ�����ƶ�
C������Ӧ���ʺ��淴Ӧ���ʶ���С��ƽ��������Ӧ�����ƶ�
D������Ӧ���ʺ��淴Ӧ���ʶ���С��ƽ�����淴Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶���11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ˮ�������c��H+��=1��10-12 mol/L�����£����и�������һ�����ܴ���������� �� ��
A��NH4����NO3����Cl����Na+ B��K+��SO32����Cl����NO3��
C��Na+��SO42����Cl����HCO3�� D��Na+��NO3����Fe3����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ�����ϵ��Ĵ��¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
������������ȷ����( )
A��������ʹ���Ը��������Һ��ɫ��֤���������в����ڵ�˫������Ľṹ
B��(CH3)2C=CHCH2CH3������̼ԭ��һ������
C������ϩ��ʹ��ˮ��ɫ
D���״����Ҷ�����HOCH2CH2OH����Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶������У��ģ���ѧ�Ծ��������棩 ���ͣ�ѡ����
���й���ʳƷ���Ӽ�����������ȷ����
A����ͬʱ�����������͵�ζ�� B���������ƿ����°�
C���ҹ�Ӧ�ý�ֹʹ��ζ�� D���������ƿ�����ʳƷ�ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꺣��ʡ�߶���12�¶ο���ѧ�Ծ��������棩 ���ͣ������
��֪A(g)+B(g) C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
�¶�/�� | 700 | 800 | 830 | 1000 | 1200 |
ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
�ش��������⣺
��1���÷�Ӧ��ƽ�ⳣ������ʽK=_________________����H________0�����������������=������
��830��ʱ����һ��5L���ܱ������г���0.20mol��A��0.80mol��B���練Ӧ��ʼ6s��A��ƽ����Ӧ����v��A��=0.003mol•L-1•s-1����6sʱc(A)Ϊ________ mol/L��C�����ʵ���Ϊ_____mol������Ӧ����һ��ʱ��ﵽƽ��ʱA��ת����Ϊ___________�������ʱ����ܱ��������ٳ���1mol�����ƽ��ʱA��ת����Ϊ________��
��3���жϸ÷�Ӧ�Ƿ�ﵽƽ�������Ϊ_________������ȷѡ��ǰ����ĸ����
a��ѹǿ����ʱ��ı� b��������ܶȲ���ʱ��ı�
c��c(A)����ʱ��ı� d����λʱ��������C��D�����ʵ������
��4��1200��ʱ��ӦC(g)+D(g) A(g)+B(g)��ƽ�ⳣ����ֵΪ________��
A(g)+B(g)��ƽ�ⳣ����ֵΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꺣��ʡ��һ��12�¶ο���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ǵĺ�ˮ�Ƴ�����ˮ����ȷ�ķ�����
A������ B������
C���ȹ��˺����� D������ij��ҩƷ�ܽ���ǵĹ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ɹų����и߶��ϵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�к�̼Ԫ�ص�����������ͬ��A��B������������A��B����������ȷ����
A�����߲�������ͬϵ��
B������һ����ͬ���칹��
C����1mol��A��B�ֱ�ȼ������CO2������һ�����
D���������ʽ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�ڵ��Ĵε��л�ѧ�Ծ��������棩 ���ͣ������
CO2��CH4��������Ҫ���������壬ͨ��CH4��CO2��Ӧ�������ֵ�Ļ�ѧƷ��Ŀǰ���о�����
��1����֪��CH4��g��+2O2��g��=CO2��g��+2H2O��g����H1=a kJ•mol-1
CO��g��+H2O ��g��=CO2��g��+H2 ��g����H2=b kJ•mol-1
2CO��g��+O2��g��=2CO2��g����H3=c kJ•mol-1
��ӦCO2��g��+CH4��g�� 2CO��g��+2H2��g�� �ġ�H=_________��
2CO��g��+2H2��g�� �ġ�H=_________��
��2����һ�ܱ�������ͨ�����ʵ���Ũ�Ⱦ�Ϊ0.1mol/L��CH4��CO2����һ�������·���������Ӧ�����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ����ͼ��
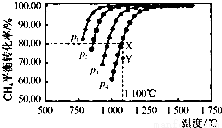
���жϸ÷�Ӧ�ġ�H________0���������������=����
��ѹǿP1��P2��P3��P4 �ɴ�С��˳��Ϊ________________
��1100��÷�Ӧ��ƽ�ⳣ��Ϊ_________������С�����һλ��
���ڲ��ı䷴Ӧ��������ǰ���£���ȡ������ʩ��Y��ƽ����ϵת��ΪX�㣬��ת�������У����б仯��ȷ����________������ţ�
a��v(��)һֱ���� b��v(��)һֱ����
c��v(��)�ȼ�С������ d��v(��)�ȼ�С������
��3����Cu2Al2O4Ϊ���������Խ�CO2��CH4ֱ��ת��Ϊ���ᡣ
�ٸ÷�Ӧ�Ļ�ѧ����ʽΪ____________________
�ڽ�Cu2Al2O4�ܽ���ϡ�����еĻ�ѧ����ʽΪ____________________
(4)��CO2Ϊԭ�Ͽ��Ժϳɶ������ʡ�
������FeO����CO2�Ļ�ѧ����ʽΪ��6 FeO+CO2=2Fe3O4+C����Ӧ��ÿ����1 mol Fe3O4��ת�Ƶ��ӵ����ʵ���Ϊ_______mol��
������������ˮ��Һ������ʽ��е�⣬��ͭ�缫��CO2��ת��ΪCH4����һ�缫ʯī���ӵ�Դ��_____������õ�ⷴӦ���ܻ�ѧ����ʽΪ____________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com