
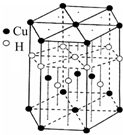
 [Cu(NH3)4]SO4•H2O是一种杀虫剂.
[Cu(NH3)4]SO4•H2O是一种杀虫剂.分析 (1)Cu是29号元素,其3d能级上有10个电子、4s能级上有1个电子,根据构造原理书写Cu原子核外电子排布式;Cu属于ds区;
(2)同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,且第IIA族、第VA族元素第一电离能大于其相邻元素,同一主族元素,元素第一电离能随着原子序数增大而减小;
(3)氢键能增大物质的溶解性;
(4)肼分子中每个N原子形成3个化学键且每个N原子含有1个孤电子对,根据价层电子对互斥理论确定N原子杂化方式;
(5)硫酸根离子价层电子对个数=4+$\frac{6+2-4×2}{2}$=4,根据价层电子对互斥理论确定硫酸根离子空间构型;原子个数相同、价电子数相等的微粒互为等电子体;
(6)根据均摊法确定各元素原子个数,从而确定其化学式.
解答 解:(1)Cu是29号元素,其3d能级上有10个电子、4s能级上有1个电子,根据构造原理书写Cu原子核外电子排布式[Ar]3d104s1;Cu属于ds区,
故答案为:[Ar]3d104s1;ds;
(2)同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,且第IIA族、第VA族元素第一电离能大于其相邻元素,同一主族元素,元素第一电离能随着原子序数增大而减小,所以这三种元素第一电离能大小顺序是N>O>S,故答案为:N>O>S;
(3)H2O与H2O2之间能形成氢键导致双氧水易溶于水,故答案为:H2O与H2O2之间形成氢键;
(4)肼分子中每个N原子形成3个化学键且每个N原子含有1个孤电子对,根据价层电子对互斥理论确定N原子杂化方式为sp3,故答案为:sp3;
(5)硫酸根离子价层电子对个数=4+$\frac{6+2-4×2}{2}$=4,根据价层电子对互斥理论确定硫酸根离子空间构型为正四面体;原子个数相同、价电子数相等的微粒互为等电子体,与硫酸根离子互为等电子体的有CCl4或SiCl4或SO2Cl2;
故答案为:正四面体;CCl4或SiCl4或SO2Cl2;
(6)该晶胞中Cu原子个数=3+12×$\frac{1}{6}$+2×$\frac{1}{2}$=6,H原子个数=4+6×$\frac{1}{3}$=6,所以其化学式为CuH,
故答案为:CuH.
点评 本题考查物质结构和性质,为高频考点,涉及晶胞计算、微粒空间构型判断、原子杂化方式判断、元素周期律、原子核外电子排布等知识点,侧重考查学生分析计算及空间想象能力,明确基本原理、元素周期律及晶胞计算方法是解本题关键,注意该晶胞中每个顶点上的原子被6个晶胞占有而不是8个晶胞占有,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 在空气中敞口久置的浓硫酸,溶液质量增大(难挥发性) | |
| B. | 在加热条件下铜与浓硫酸反应(强氧化性、酸性) | |
| C. | 蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性) | |
| D. | 浓硫酸与少量胆矾晶体混合,晶体由蓝色变成白色(脱水性) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
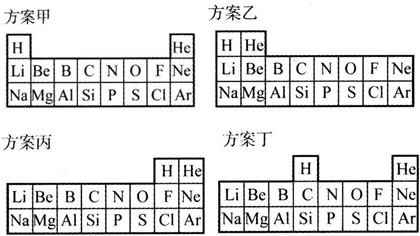
| “合理”的理由 | |
| 方案甲 | |
| 方案乙 | |
| 方案丙 | |
| 方案丁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属表面的氧化膜都很致密,能对金属起到保护作用 | |
| B. | 金属表面的氧化膜的形成都需要金属暴露在空气中很长时间才会形成 | |
| C. | 金属表面的氧化膜薄层的厚度会随着金属暴露在空气中的时间增长而加厚 | |
| D. | 某些金属表面氧化膜的形成对这些金属的广泛应用起到关键作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为倍受青睐的清洁燃料. |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障. |
| C | 植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂. |
| D | 室温下其单质呈粉末固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰. |
| E | 它是人体不可缺少的微量元素,其单质也是工业生产中不可缺少的金属原材料,常用于制造桥梁、轨道等. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在相同条件下的溶解度:NaHCO3>Na2CO3 | |
| B. | 热稳定性:HF>HCl>HBr>HI | |
| C. | 氧化性:F2>Cl2>Br2>I2 | |
| D. | 碳酸钠溶液与稀盐酸互滴时,两种操作现象不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑦⑧⑨ | B. | ②④⑦⑨ | C. | ③④⑦ | D. | ④⑤⑦⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉溶液中加入少许食醋可以增强其漂白效果 | |
| B. | 用二氧化硫漂白米粉是违法行为,因为二氧化硫有毒 | |
| C. | 铝制品在生活中非常普遍,这是因为铝不活泼 | |
| D. | 氢氧化铝可用于治疗胃酸过多,但不宜长期服用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol Na2CO3和1.6mol NaOH | B. | 1mol Na2CO3与0.6mol NaHCO3 | ||
| C. | 0.8mol Na2CO3和1mol NaOH | D. | 1mol Na2CO3和0.6mol NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com