
把淀粉和NaCl溶液装入半透膜袋内,浸入蒸馏水中进行渗析。试回答:
(1)证明淀粉未透过半透膜而Cl-已透过半透膜的实验方法是_______________ ___________________________________________________________________________。
(2)证明淀粉与NaCl溶液已分离完全的实验方法是___________________________。
科目:高中化学 来源: 题型:
已知化学反应2C(固)+O2(气) 2CO(气)和2CO(气)+O2(气)
2CO(气)和2CO(气)+O2(气) 2CO2(气)都是放热反应。据此判断,下列说法中不正确的是(其他条件均相同)( )
2CO2(气)都是放热反应。据此判断,下列说法中不正确的是(其他条件均相同)( )
A.12 g C所具有的能量一定高于28 g CO所具有的能量
B.56 g CO和32 g O2所具有的总能量大于88 g CO2所具有的能量
C.12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量
D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质相互混合反应后,最终有白色沉淀生成的是
①金属钠投入FeCl2溶液中 ②过量NaOH溶液和明矾溶液混合 ③少量Ca(OH)2投入过量NaHCO3溶液中 ④向NaAlO2溶液中通入过量CO2 ⑤向饱和Na2CO3溶液中通入过量CO2
A.①③④⑤ B.①④ C.②③ D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
硫代硫酸钠是一种重要的化工产品。工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程。
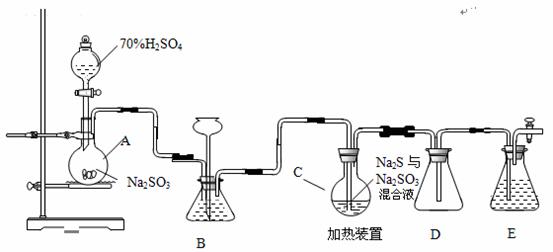
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (II)
S(s)+Na2SO3(aq)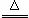 Na2S2O3(aq) (III)
Na2S2O3(aq) (III)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若 ,则整个装置气密性良好。装置D的作用是 。装置E中为 溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)实验中,为使SO2缓慢进入烧瓶C,采用的操作是 。
(5)已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是 。
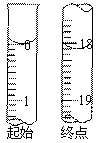 (6)反应终止后,烧瓶C中的溶液经蒸发浓缩冷却,过滤,洗涤,干燥,即得到粗产品(主要含有Na2S2O3•5H2O和其他杂质)。某兴趣小组为测定该产品纯度,准确称取4.96 g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L¯1碘的标准溶液滴定。反应原理为:2S2O32-+I2=S4O62-+2I¯,滴定至终点时,滴定起始和终点的液面位置如下图,则产品的纯度为_________。经仪器分析,该产品纯度为16%,分析该兴趣小组测定产品纯度偏差的原因(忽略人为误差)
(6)反应终止后,烧瓶C中的溶液经蒸发浓缩冷却,过滤,洗涤,干燥,即得到粗产品(主要含有Na2S2O3•5H2O和其他杂质)。某兴趣小组为测定该产品纯度,准确称取4.96 g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L¯1碘的标准溶液滴定。反应原理为:2S2O32-+I2=S4O62-+2I¯,滴定至终点时,滴定起始和终点的液面位置如下图,则产品的纯度为_________。经仪器分析,该产品纯度为16%,分析该兴趣小组测定产品纯度偏差的原因(忽略人为误差)
。
[M(Na2S2O3•5H2O)=248g/mol]
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关胶体和溶液的比较中,正确的是( )
A.溶液呈电中性,胶体带有电荷
B.溶液可透过滤纸,胶体不可透过滤纸
C.溶液中通过光束没有特殊现象,胶体中通过光束有丁达尔现象
D.胶体与溶液的本质区别是胶体有丁达尔现象
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应的离子方程式:
(1)铁粉加入CuSO4溶液中:
________________________________________________________________________,
(2)Cl2通入石灰水中:
________________________________________________________________________,
(3)漂白粉溶液与空气中CO2反应:
________________________________________________________________________,
(4)向沸水中滴加少量FeCl3溶液制备Fe(OH)3胶体:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是实验室制取并验证SO2的某些性质的装置图。试回答:
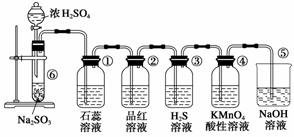
(1)在⑥中发生反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(2)在①中的实验现象为___________________________________________________,
此实验证明SO2是________气体。
(3)②中的品红溶液_____________________________________________________,
证明SO2有________________。
(4)③中的实验现象是_____________________________________________________,
证明SO2有____________性。
(5)④中的实验现象是___________________________________________________,
证明SO2有____________性。
(6)⑤的作用是_________________________________________________________,
反应的化学方程式为_____________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com