(2013?潍坊模拟)TiO
2在工业生产和日常生活中有生果用途.
(1)工业上用钛矿石(FeTiO
3,含FeO、Al
2O
3、SiO
2等杂质)经过下述反应制得:

其中,步骤②发生的反应为:2H
2SO
4+FeTiO
3═TiOSO
4+FeSO
4+2H
2O.
①净化钛矿石时,是否需要除云杂质FeO?答:
不需要
不需要
(填“需要”或“不需要”).
②净化钛矿石时,需用浓氢氧化钠溶液来处理.写出该过程中发生反应的化学方程式:
Al2O3+2NaOH=2NaAlO2+H2O;SiO2+2NaOH=Na2SiO3+H2O
Al2O3+2NaOH=2NaAlO2+H2O;SiO2+2NaOH=Na2SiO3+H2O
.
(2)TiO
2可通过下述两种方法制备金属钛;
方法一是电解TiO
2来获得Ti(同时产生O
2-):将处理过的TiO
2作阴极,石墨为阳极,熔融CaCl
2为电解液,用炭块作电解槽池.
(3)阴极反应的电极反应式为
TiO2+4e-=Ti+2O2
TiO2+4e-=Ti+2O2
.
(4)电解过程中需定期向电解槽池中加入炭块的原因是
碳单质会与阳极产生的氧气反应而不断减少
碳单质会与阳极产生的氧气反应而不断减少
.
方法二是先将TiO
2与Cl
2、C反应得到TiCl
4,再用镁还原得到Ti.因下述反应难于发生:
TiO
2(s)+2Cl
2?(g)?TiCl
4(l)+O
2(g)△H=151kJ/mol
所以不能直接由TiO
2与Cl
2反应(即氯化反应)来制取TiO
4.当往氯化反应体系中加入炭块后,炭块与上述反应发生耦合,使得反应在高温条件下能顺利进行.
(5)已知:C(s)+O
2(g)═CO
2(g)△H=-394kJ/mol.请填空:
TiO
2(s)+C(s)+2Cl
2(g)═TiCl
4(l)+CO
2(g)△H=
-243KJ?mol-1
-243KJ?mol-1
.
(6)从化学平衡的角度秋:往氯化反应体系中加入炭块时,氯化反应能顺利进行的原因是
碳单质与氧气反应减小产物浓度,使平衡向右移动,导致反应顺利进行;碳与氧气反应放热,相当于升高温度,平衡向着右移动
碳单质与氧气反应减小产物浓度,使平衡向右移动,导致反应顺利进行;碳与氧气反应放热,相当于升高温度,平衡向着右移动
.




 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案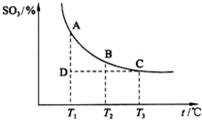 (2013?潍坊模拟)如图,研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义.
(2013?潍坊模拟)如图,研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义.