
【题目】①某NaCl样品中可能含有SO42﹣ , CO32﹣ , 为检验杂质离子的存在,采取如下实验步骤:样品 ![]()
![]() 无明显现象
无明显现象 ![]() 无明显现象.则加入的试剂A为 , B为(填化学式),该现象证明样品中不含有 .
无明显现象.则加入的试剂A为 , B为(填化学式),该现象证明样品中不含有 .
②在后续实验中需要使用450mL0.5molL﹣1NaCl溶液,为配制该浓度NaCl溶液进行实验,需用托盘天平称取NaClg.
③配制NaCl溶液时,若出现下列操作,会使配制浓度偏高的是
A.称量时NaCl已潮解
B.天平砝码已锈蚀
C.定容时俯视刻度线
D.定容摇匀后液面下降,又加水至刻度.
【答案】盐酸;氯化钡;CO32﹣、SO42﹣;14.6;BC
【解析】解:①取样品溶解,加入足量稀盐酸,无气泡产生,说明样品中不含碳酸根,再加入氯化钡溶液,无白色沉淀产生,说明溶液中不含硫酸根,
故答案为:盐酸;氯化钡;CO32﹣、SO42﹣;
②容量瓶的规格没有450mL,应选500mL配制,则需氯化钠的物质的量为:n=cV=0.50mol/L×0.5L=0.25mol,氯化钠的质量为:m=nM=0.25mol×58.5g/mol=14.625g,托盘天平应保留1位小数,氯化钠的质量为14.6g,
故答案为:14.6;
③A.称量时NaCl已潮解,溶质偏少,浓度偏低,故A错误;
B.天平砝码生锈,所称溶质氯化钠质量偏大,浓度偏高,故B正确;
C.定容时,俯视读取刻度,导致溶液体积偏小,溶液浓度偏高,故C正确;
D.定容摇匀后液面下降,是正常现象,又加水至刻度,导致溶液体积偏大,溶液浓度偏低,故D错误;
故答案为:BC.
①用稀盐酸检验碳酸根的存在,再用氯化钡检验硫酸根的存在;
②容量瓶的规格没有450mL,应选500mL配制,依据n=cV计算物质的量,再计算出质量;
③分析操作对溶质的物质的量n和溶液的体积V,依据c=![]() 进行误差分析,凡是使n偏大或者使V偏小的操作,溶液浓度偏高,凡是使n偏小或者V偏大的操作,溶液浓度偏低.
进行误差分析,凡是使n偏大或者使V偏小的操作,溶液浓度偏高,凡是使n偏小或者V偏大的操作,溶液浓度偏低.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】恒容密闭容器中存在下列平衡:CO(g)+H2O(g)CO2(g)+H2(g).CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法错误的是( ) 
A.在T2时,若反应进行到状态D,则一定有v正<v逆
B.平衡状态A与C相比,平衡状态A的c(CO)小
C.若T1、T2时的平衡常数分别为K1、K2 , 则K1<K2
D.反应CO(g)+H2O(g)CO2(g)+H2(g)的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)CO2(g)+H2(g)△H>0
试回答下列问题:
(1)请写出该化学反应的平衡常数表达式: .
(2)830K温度下,若起始时c(CO)=2molL﹣1 , c(H2O)=3molL﹣1 , 达到平衡时CO的转化率为50%,则在该温度下,该反应的平衡常数K= .
(3)若降低温度,该反应的K值将 , 该反应的正反应速率将; 该反应的逆反应速率将(均填“增大”“减小”或“不变”).
(4)若要提高CO的转化率,可采取的措施有: .
(5)830K温度下,若起始时c(CO)=1molL﹣1 , c(H2O)=2molL﹣1 , 反应进行一段时间后,测得H2的浓度为0.5molL﹣1 , 则此时该反应是否达到平衡状态(填“是”与“否”),你判断的依据是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于摩尔质量的叙述正确的是( )
A. 氢气的摩尔质量是2 g B. 氢气的摩尔质量就是其相对分子质量
C. 氢的摩尔质量是2 g/mol D. 氢气的摩尔质量是2 g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流电池是一种新型的绿色环保储能电池,该电池性能优良,其电池总反应为:V3++VO2++H2O ![]() VO2++2H++V2+ . 下列叙述正确的是( )
VO2++2H++V2+ . 下列叙述正确的是( )
A.放电过程中电解质溶液中阴离子移向正极
B.放电时每转移0.5mol电子,负极有0.5molV2+被氧化
C.充电时阳极附近溶液的酸性减弱
D.充电时阳极反应式为:VO2++2H++e﹣═VO2++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是( )
A.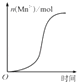
表示10 mL 0.01molL﹣1KMnO4酸性溶液与过量的0.1molL﹣1 H2C2O4溶液混合时,n(Mn2+)随时间的变化(Mn2+对该反应有催化作用)
B.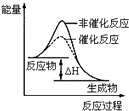
表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.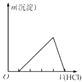
表示示向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸所得沉淀物质的量与盐酸体积的关系
D.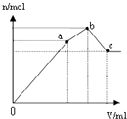
表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A.淀粉、纤维素、蛋白质均为高分子
B.麦芽糖属于双糖,能发生银镜反应
C.油脂、氨基酸、蔗糖都能发生水解
D.通常情况下,强酸、强碱或高温条件均可使酶失去活性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O3在化学定量分析中常用作基准物质,遇酸易分解;实验室制备原理为2Na2S+Na2CO3+4SO2 ![]() 3Na2S2O3+CO2 . 实验装置如下:
3Na2S2O3+CO2 . 实验装置如下: 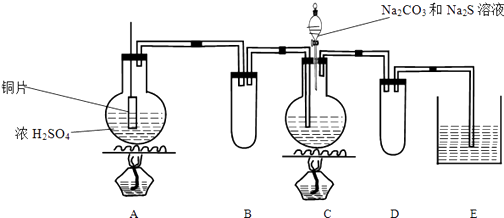
(1)A中发生反应的化学方程式是: .
(2)E中所盛试剂作用是;若要停止A中的化学反应,还可以采取的操作是 .
(3)B和D装置作用:
(4)甲同学在加热A后,发现液面下的铜丝变黑.该同学对黑色生成物提出如下假设:
①可能是CuO;②可能是Cu2O;③可能是CuS
乙同学认为假设②一定不成立,依据是 .
该同学设计实验进一步验证黑色物质的组成: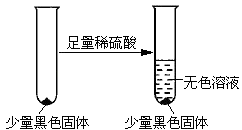
基于上述假设分析,黑色物质的组成为(填化学式) .
(5)C中通入SO2不能过量原因是 .
(6)实验室用硫代硫酸钠溶液吸收残余氯气生成SO42﹣ , 其反应的离子方程式是:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com