
| A.V(酸)=102V(碱) | B.V(碱)=102V(酸) |
| C.V(酸)=2V(碱) | D.V(碱)=2V(酸) |
科目:高中化学 来源:不详 题型:单选题
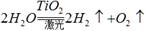 。有下列几种说法:① 水分解反应是放热反应;②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件;③ 使用氢气作燃料有助于控制温室效应;④氢气是一级能源。其中叙述正确的是
。有下列几种说法:① 水分解反应是放热反应;②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件;③ 使用氢气作燃料有助于控制温室效应;④氢气是一级能源。其中叙述正确的是 | A.①② | B.③④ | C.②③ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.用标准溶液润洗滴定管2~3次 |
| B.取标准KOH溶液注入碱式滴定管至刻度0以上2~3cm |
| C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液 |
| D.调节液面至0或0以下刻度,记下读数 |

| 实验次数 | c(KOH)/mol·L-1 | B中起点刻度 | B中终点刻度 | V(HCl)/ml |
| 1 | 0.1000 | 0 | 24.95 | 25.00 |
| 2 | 0.1000 | 0 | 24.96 | 25.00 |
| 3 | 0.1000 | 0 | 24.50 | 25.00 |
| 4 | 0.1000 | 0 | 24.94 | 25.00 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.7 | B.2.0 | C.12.0 | D.12.4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CH3OH(l) + 3/2O2(g) ="=" CO2(g) + 2H2O(l); △H =" +726.5KJ/mol" |
| B.CH3OH(l) + 3/2O2(g) ="=" CO2(g) + 2H2O(l); △H =" -726.5KJ/mol" |
| C.CH3OH(l) + 3/2O2(g) ="=" CO2(g) + 2H2O(g); △H =" -675.3KJ/mol" |
| D.2CH3OH(l) + 3O2(g) ="=" 2CO2(g) + 4H2O(l); △H = -1453KJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液呈中性,可选用甲基橙或酚酞作指示剂 | B.溶液呈中性,只能选用石蕊作指示剂 |
| C.溶液呈碱性,可选用甲基橙或酚酞作指示剂 | D.溶液呈碱性,只能选用酚酞作指示剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
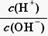 =1010,请回答下列问题:
=1010,请回答下列问题:A.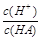 | B.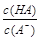 | C.c(H+)·c(OH-) | D.c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H++OH-,向右移动且溶液呈碱性的是( )
H++OH-,向右移动且溶液呈碱性的是( )| A.向水中加入NaHSO4溶液 | B.向水中加入少量金属钠 |
| C.向水中加入NaOH溶液 | D.将水加热到100℃,使pH=6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com