
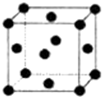
 X��Y��Z��W��R����Ϊǰ������Ԫ����ԭ��������������X�Ļ�̬ԭ�Ӻ�����7�ֲ�ͬ�˶�״̬�ĵ��ӣ�Yԭ���������2�ԳɶԵ��ӣ�Z��ԭ������ΪY��ԭ��������2����W3+�Ļ�̬����3d���Ϊ�����״̬��R��������������Һ�����ڼ��������ǵĴ��ڣ�
X��Y��Z��W��R����Ϊǰ������Ԫ����ԭ��������������X�Ļ�̬ԭ�Ӻ�����7�ֲ�ͬ�˶�״̬�ĵ��ӣ�Yԭ���������2�ԳɶԵ��ӣ�Z��ԭ������ΪY��ԭ��������2����W3+�Ļ�̬����3d���Ϊ�����״̬��R��������������Һ�����ڼ��������ǵĴ��ڣ�| 1 |
| 2 |
| 1 |
| 8 |
| 5+1-2��3 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
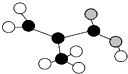 ij����������ij��Ʒֻ��C��H��O����Ԫ�أ������ģ����ͼ��ʾ��ͼ��������֮������ߴ�����ѧ�����絥����˫���ȣ������жԸò�Ʒ����������ȷ���ǣ�������
ij����������ij��Ʒֻ��C��H��O����Ԫ�أ������ģ����ͼ��ʾ��ͼ��������֮������ߴ�����ѧ�����絥����˫���ȣ������жԸò�Ʒ����������ȷ���ǣ�������| A��������Ϊ̼̼˫�����Ȼ� |
| B����CH2=CHCOOCH3��Ϊͬ���칹�� |
| C���ܷ���������Ӧ |
| D������������ԭ�ӿ�����ͬһƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
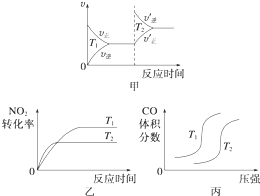 ����β���к���CO��NO2���ж����壬��������װβ������װ�ã���ʹ�ж��������Ӧת��Ϊ�����壮
����β���к���CO��NO2���ж����壬��������װβ������װ�ã���ʹ�ж��������Ӧת��Ϊ�����壮| ��ʼ���ʵ��� | �� | �� | �� |
| n��H2O��/mol | 0.10 | 0.20 | 0.20 |
| n��CO��/mol | 0.10 | 0.10 | 0.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ũ��/mol?L-1 ʱ��/min |
NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| CaCO3 | CaSO4 | Mg��OH��2 | MgCO3 |
| 1.4��10-3 | 2.55��10-2 | 9��10-4 | 1.1��10-2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NaOH |
| B��AgNO3 |
| C��KI |
| D��Na2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ij�ε�ˮ��Һ�����ԣ�����һ����ǿ�������� |
| B������ˮ��Ĺ����ƻ���ˮ�ĵ���ƽ�� |
| C������ʱ��AgCl������Һ�м���AgNO3���壬c��Cl-������ |
| D������ʱpH=3����Һ��pH=11����Һ��������������Һһ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | ��ѧ��Ӧ�������ӷ���ʽ | ���� |
| 1 | ����������ˮ��CH3COO-+H2O�TCH3COOH+OH- | ��ȷ |
| 2 | ������������Һ�еμ������Ȼ�����Al3++3OH-�TAl��OH��3�� | ����Al��OH��3�������������� |
| 3 | �����뵽������ϡ������Һ�У�3Fe+8H++2NO3-�T3Fe2++2NO��+4H2O | ��ȷ |
| 4 | ������������Һ�еμ�����������Һ�����������ʵ�����ࣺ 3Ba2++6OH-+2Al3++3SO42-�T3BaSO4��+2Al��OH��3�� |
����Al3+��OH-�Ļ�ѧ������֮��Ϊ1��3 |
| A��1 | B��2 | C��3 | D��4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com