
下列溶液中各微粒的浓度关系不正确的是
A.0.1 mol/LCH3COOH溶液中:c(CH3COO-)+ c(CH3COOH)=0.1mol/L
B.CH3COONa溶液中:c(Na+)> c(CH3COO-)> c(OH-)> c(H+)
C.Na2S溶液中:2 c(Na+)= c(S2-) + c(HS-)+ c(H2S)
D.NaHCO3溶液中: c(OH-) = c(H+) + c(H2CO3)-c(CO32-)
C
【解析】
试题分析:A、CH3COOH溶液中根据醋酸根守恒可知,c(CH3COO-)+c(CH3COOH)=0.1mol/L,故A正确;B、CH3COONa溶液中,CH3COONa═CH3COO-+Na+,因醋酸根离子水解显碱性,则c(Na+)>c(CH3COO-)、c(OH-)>c(H+),水解的程度不大,则c(CH3COO-)>c(OH-),故B正确;C、Na2S溶液,n(Na)=2n(S),由物料守恒可知,1/2c(Na+)=c(S2-)+c(HS-)+c(H2S),故C错误;D、NaHCO3溶液不显电性,所以阳离子带的正电荷总数等于阴离子带的负电荷总数,则c(H+)+c(Na+)=2c(CO32-)+c(HCO3-)+c(OH-),故D正确,所以选C.
考点:溶液的物料守恒,离子的电荷守恒。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源:2015届甘肃省高三第一次诊断考试化学试卷(解析版) 题型:选择题
氢化钙(CaH2)可作为生氢剂,反应的化学方程式为CaH2+2H2O=Ca(OH)2+2H2↑,下列说法不正确的是
A.CaH2是还原剂,又是氧化剂
B.H2既是氧化产物,又是还原产物
C.CaH2是还原剂,H2O是氧化剂
D.氧化产物与还原产物质量比为1∶1
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省天水市高三上学期期中考试化学试卷(解析版) 题型:选择题
将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是
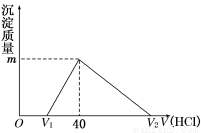
A.原合金质量为0.92 g B.标准状况下产生氢气896 mL
C.图中V2为60 mL D.图中m值为1.56 g
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省天水市高二上学期期中考试化学(理)试卷(解析版) 题型:实验题
(14分)碘溶于碘化钾溶液中形成I3-,并建立如下平衡:I3- I-+ I2。实验室可以通过氧化还原滴定法测定平衡时I3-的浓度。
I-+ I2。实验室可以通过氧化还原滴定法测定平衡时I3-的浓度。
实验原理:
为了测定平衡时的c(I3-),可用过量的碘与碘化钾溶液一起摇动,达平衡后取上层清液用标准的Na2S2O3滴定:2 Na2S2O3 + I2 = 2NaI + Na2S4O6。由于溶液中存在I3- I-— + I2的平衡,所以用硫代硫酸钠溶液滴定,最终测得的是I2和I3-—的总浓度,设为c1,c1 = c(I2)+c(I3-);c(I2) 的浓度可用相同温度下,测过量碘与水平衡时溶液中碘的浓度代替,设为c2,则c(I2)= c2,c(I3-)=c1 —c2;
I-— + I2的平衡,所以用硫代硫酸钠溶液滴定,最终测得的是I2和I3-—的总浓度,设为c1,c1 = c(I2)+c(I3-);c(I2) 的浓度可用相同温度下,测过量碘与水平衡时溶液中碘的浓度代替,设为c2,则c(I2)= c2,c(I3-)=c1 —c2;
实验内容:
(1).用一只干燥的100 mL 碘量瓶(测量过程中所用的一种密闭玻璃容器)和一只250 mL碘量瓶,分别标上1、2号,用量筒取80 mL 0.0100 mol.L-1 KI于1号瓶,取200 mL 蒸馏水于2号瓶,并分别加入0.5 g过量的碘。
(2).将两只碘量瓶塞好塞子,振荡30分钟,静置。
(3).分别取上层清液20 mL用浓度为c mol/L标准Na2S2O3溶液进行滴定。1号瓶消耗V1 mL Na2S2O3溶液,2号瓶消耗V2 mL Na2S2O3溶液。
(4).带入数据计算c(I3—)
试回答下列问题
①标准Na2S2O3溶液应装入 (填“酸式滴定管”或“碱式滴定管”),原因是 。
②碘量瓶在震荡静置时要塞紧塞子,可能的原因是 。
③滴定时向待测液中加入的指示剂是 ,到达滴定终点时的现象为 。
④用c 、V1 和V2 表示c(I3-)为 mol·L-1。
⑤若在测定1号瓶时,取上层清液时不小心吸入了少量的I2固体,则测定的c(I3-)
(填“偏大”、“偏小”或“不变”)
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省天水市高二上学期期中考试化学(理)试卷(解析版) 题型:选择题
在0.1 mol·L-1CH3COOH溶液中存在如下电离平衡:CH3COOH  CH3COO一+ H+,对于该平衡,下列叙述不正确的是
CH3COO一+ H+,对于该平衡,下列叙述不正确的是
A.加入水时,平衡向正反应方向移动,溶液中n(H+)增大
B.加入少量冰醋酸,平衡向正反应方向移动,溶液中c(H+)增大
C.加入少量0.1 mol·L-1HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向逆反应方向移动,溶液中c(H+)减小
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省天水市高二上学期期中考试化学(理)试卷(解析版) 题型:选择题
下列有关说法正确的是
A.反应NH3(g)+HCl(g)= NH4Cl(s)在室温下可自发进行,则该反应的△H<0
B.当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀
C.CH3COOH溶液加水稀释后,电离平衡正向移动,溶液中的c(CH3COO-)增大
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省天水市高二上学期期中考试化学(文)试卷(解析版) 题型:填空题
(6分)我国农业因遭受酸雨而造成的损失每年高达15亿多元,为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。
现有雨水样品1份,每隔一段时间测定该雨水样品的pH所得数据如下:
测试时间/h | 0 | 1 | 2 | 3 | 4 |
雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
分析数据,回答以下问题:
如果将刚取样的上述雨水和自来水混和,PH将变 。(填“大”、“小”、“不变”)
你认为减少酸雨产生的途径可采用的措施是 。
①少用煤作燃料 ②把工厂烟囱造高 ③燃烧脱硫
④在已酸化的土壤中加石灰 ⑤开发新能源
A.①③⑤ B.②③④⑤ C.①②⑤ D.①②③
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省天水市高二上学期期中考试化学(文)试卷(解析版) 题型:选择题
关于生铁和钢的描述正确的是
A.生铁是铁碳混合物,钢是纯铁、纯净物
B.钢的性能不如生铁优越,使用范围不如生铁广
C.生铁和钢是含碳量不同的两种铁碳的合金
D.生铁和钢的主要成分都是铁,性能相近
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高三9月月考化学试卷(解析版) 题型:选择题
中学常见物质A、B、C、D、E、X,存在图转化关系(部分生成物和反应条件略去)。下列推断不正确的是
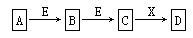
A、若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
B、若D是一种强碱,则A、B、C均可与X反应生成D
C、若D为NaCl,且A可与C反应生成B,则E可能是CO2
D、若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com