
【题目】按要求填空:
(1)在室温下,等体积、等浓度的氢氧化钠与醋酸混合后溶液呈__性,溶液中c(Na+)__c(CH3COO-)(填“>”“=”或“<”);pH=13的氢氧化钠与pH=1的醋酸等体积混合后溶液呈__性,溶液中c(Na+)___c(CH3COO-)(填“>”“=”或“<”);
(2)下列溶液,①0.1mol/L HCl溶液②0.1mol/L H2SO4溶液③0.1mol/L NaOH溶液④0.1mol/L CH3COOH溶液,按pH由小到大顺序为___。
(3)CuSO4的水溶液呈酸性的原因是(用离子方程式表示):____;实验室在配制CuSO4的溶液时,常将CuSO4固体先溶于较浓的硫酸中,然后再用蒸馏水稀释到所需的浓度,以___(填“促进”、“抑制”)其水解。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,充分反应后溶液呈中性,则反应后溶液存在的离子有____,其浓度由大到小的顺序为_____,氨水的浓度a__0.01 mol·L-1(填“>”、“ <”或“=”)。
(5)已知:难溶电解质Cu(OH)2在常温下的KSP=2×10-20,则常温下:某CuSO4溶液中c(Cu2+)=0.02molL-1,如要生成Cu(OH)2沉淀,应调整溶液的pH最小为____。
(6)某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:
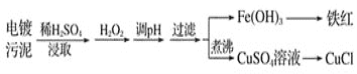
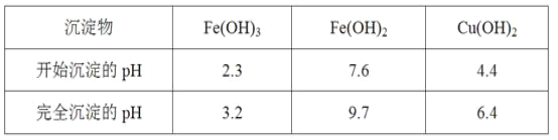
①酸浸后加入H2O2的目的是_____________,调pH的最适宜范围为_______。
②调pH过程中加入的试剂最好是_________。
A.NaOH B.CuO C.NH3·H2O D.Cu2(OH)2CO3
③煮沸CuSO4溶液的原因是_____;向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,反应的化学方程式________。
【答案】碱 > 酸 < ②①④③ Cu2++2H2O![]() Cu(OH)2+2H+ 抑制 H-、H+、NH4+、Cl- c(Cl-)=c(NH4+)>c(H+)=c(OH-) > 5 将Fe2+氧化为Fe3+,便于调整pH使其与Cu2+分离 3.2~4.4 BD 除净溶液中的H2O2,避免影响下一步CuCl的生成 2CuSO4+2NaCl+Na2SO3+H2O=2CuCl↓+Na2SO4+H2SO4
Cu(OH)2+2H+ 抑制 H-、H+、NH4+、Cl- c(Cl-)=c(NH4+)>c(H+)=c(OH-) > 5 将Fe2+氧化为Fe3+,便于调整pH使其与Cu2+分离 3.2~4.4 BD 除净溶液中的H2O2,避免影响下一步CuCl的生成 2CuSO4+2NaCl+Na2SO3+H2O=2CuCl↓+Na2SO4+H2SO4
【解析】
(1)等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,恰好生成醋酸钠,由化学式可知,阴阳离子之比为1:1,醋酸根离子水解显碱性,则c(Na+)>c(CH3COO),pH=13的氢氧化钠,其浓度为0.1mol/L,pH=1的醋酸,其浓度大于0.1mol/L,等体积混合后,醋酸过量;根据电荷守恒可知,c(Na+)+c(H+)=c(OH-)+c(CH3COO-),醋酸过量,溶液呈酸性,所以c(H+)>c(OH-),则c(Na+)<c(CH3COO);
(2)①HCl是强电解质,所以0.1mol/L HCl溶液中氢离子浓度为0.1mol/L;②硫酸是二元强酸,所以0.1mol/L H2SO4溶液中氢离子浓度为0.2mol/L;③NaOH是一元强碱,氢离子浓度最小,0.1mol/L NaOH溶液中氢离子浓度为1013mol/L;④醋酸是一元弱酸,部分电离,所以0.1mol/L CH3COOH溶液中氢离子浓度小于0.1mol/L,则这四种溶液中氢离子浓度大小顺序是③④①②,氢离子浓度越小,pH越大,则pH由小到大顺序为②①④③;
(3)CuSO4是强酸弱碱盐,铜离子水解方程式为Cu2++2H2O![]() Cu(OH)2+2H+,水解后溶液中c(H+)>c(OH),所以溶液呈酸性,即常温下pH<7;为防止CuSO4水解,所以配制CuSO4溶液时将CuSO4先溶于较浓的硫酸中,抑制其水解,然后稀释。
Cu(OH)2+2H+,水解后溶液中c(H+)>c(OH),所以溶液呈酸性,即常温下pH<7;为防止CuSO4水解,所以配制CuSO4溶液时将CuSO4先溶于较浓的硫酸中,抑制其水解,然后稀释。
(4)在一水合氨与氯化氢恰好反应生成氯化铵溶液时,铵根离子在溶液中部分水解,促进了水的电离,水的电离程度增大,溶液显酸性,当溶液显中性时,氨水稍稍过量,溶液中溶质为氯化铵和一水合氨,溶液中存在的离子为:OH、H+、NH4+、Cl;反应后的溶液显中性,则一定满足c(H+)=c(OH),根据电荷守恒c(NH4+)+c(H+)=c(Cl)+c(OH)可知:c(NH4+)=c(Cl),离子浓度大小为:c(Cl)=c(NH4+)>c(H+)=c(OH);当a=0.01时,氨水与盐酸等体积等浓度混合,两溶液恰好反应生成氯化铵溶液,铵根离子水解导致溶液显示酸性,如溶液显示中性,则氨水稍稍过量,即a>0.01,
(5)某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,则应有c(OH)![]() =
=![]() mol/L=109mol/L,则c(H+)
mol/L=109mol/L,则c(H+)![]() mol/L=105mol/L,所以pHlg(105)=5;
mol/L=105mol/L,所以pHlg(105)=5;
(6)由流程可知,加硫酸溶解后,加入过氧化氢发生2Fe2++H2O2+2H+=2Fe3++2H2O,调节pH为3.2~4.4,使铁离子转化为沉淀,过滤分离出Fe(OH)3,Fe(OH)3加热生成铁红,煮沸硫酸铜溶液,除去溶液中的过氧化氢,向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,发生2Cl-+2Cu2++SO32-=2CuCl↓+SO42-+2H+;
①根据分析,酸浸后加入H2O2的目的是将亚铁离子氧化为铁离子,便于调整pH使其与Cu2+分离;根据表格数据,调pH的最适宜范围为3.2~4.4,使铁离子转化为沉淀,过滤分离出Fe(OH)3;
②调pH过程中加入的试剂最好是CuO或Cu2(OH)2CO3,促进铁离子水解,且不引入新杂质,
答案选BD。
③煮沸CuSO4溶液的目的是除净溶液中的H2O2,避免影响下一步生成CuCl;向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,该反应的化学方程式为2CuSO4+2NaCl+Na2SO3+H2O=2CuCl↓+Na2SO4+H2SO4。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)2 mol CO(NH2)2中含_____molN原子, 所含O原子数跟________g H2O所含氧原子数相等。
(2)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______,含R的质量为1.6 g的Na2R,其物质的量为_________。
(3)CO和CO2的混合气体18 g,在标准状况下的体积为11.2 L,则混合气体的平均摩尔质量为________,混合气体中CO的质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式表示正确的是( )
A.向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO
B.AlCl3溶液中加入过量稀氨水:Al3++4NH3·H2O=AlO![]() +4NH
+4NH![]() +2H2O
+2H2O
C.稀HNO3与铁屑反应:Fe+2H+=Fe2++H2↑
D.FeCl2溶液中加入H2O2:2Fe2++H2O2+2H+=2Fe3++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取和收集纯净干燥的氯气,并进行氯气性质探究的实验装置图:

(1)反应前,在__中装浓盐酸(填写仪器名称),__中装MnO2(填写仪器名称)。
(2)装置A中所装试剂是__,目的__。装置B中所装的试剂是___,目的__。
(3)装置D中所装试剂是__,发生反应的化学方程式为__。
(4)实验室制取Cl2的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)具有复合官能团的复杂有机物,其官能团具有各自的独立性,在不同条件下所发生的化学性质可分别从各官能团讨论。如 具有四种官能团:_____、_____、___和_____(填官能团的名称)。
具有四种官能团:_____、_____、___和_____(填官能团的名称)。
(2)请同学们根据官能团的不同对下列有机物进行分类。

芳香烃:___;卤代烃:__;醇:__;酚:____;醛:___;酮:___;羧酸:__;酯:____。
(3)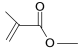 分子式为_____,结构简式为_______。
分子式为_____,结构简式为_______。
(4)有机物CH3CH(C2H5)CH(CH3)2的名称是____,![]() 的系统命名是______。
的系统命名是______。
(5)2,3-二甲基-4-乙基己烷的结构简式为 _________。
(6)2-甲基-1,3-丁二烯的键线式为______。
(7)某仅由C、H、O三种元素组成的有机化合物,经测定相对分子质量为90,取该有机化合物样品1.8g,在纯氧中完全燃烧将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g,则该有机化合物分子式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某制碱制得的纯碱中含有NaHCO3和NaCl杂质。某实验小组对此碱样品进行检查。
(1)取此碱样品10g,加热到质量不再减少,冷却称重,称得质量为9.845g,该样品中NaHCO3的质量分数为__________________________。
(2)另取10g固体样品,加蒸馏水溶解,配成250mL一定物质的量浓度的溶液,配制过程中必需使用的化学仪器有______________________(填字母)
A.烧杯 B.250mL容量瓶C.漏斗 D.胶头滴管 E.玻璃棒 F.试管
(3)量取上述配制好的溶液25mL,向其中加入过量盐酸至 不再产生气泡,共收集到190.4mL(标准状况)气体,该反应过程的离子方程式为______________________、_______________________。10g该样品中含____________gNaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示示意图,下列说法不正确的是

A. 反应的热化学方程式可表示为C(s)+H2O(g)![]() CO(g)+H2(g) ΔH=(b-a) kJ·mol-1
CO(g)+H2(g) ΔH=(b-a) kJ·mol-1
B. 该反应过程反应物断键吸收的能量一定大于生成物成键放出的能量
C. 使用催化剂无法改变该反应的ΔH
D. nmol C和n mol H2O反应生成nmol CO和nmol H2吸收的热量一定为131.3nkJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①盐酸、②铁、③碳酸氢钠、④二氧化硅是常见的物质。请回答下列问题。
(1)上述4种物质中属于盐的是______ (填序号,下同);水溶液能使紫色石蕊溶液变红的是______ 。
(2)写出盐酸的电离方程式___________。
(3)写出二氧化硅与氢氧化钠溶液反应的化学方程式_____________。
(4)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为_______。等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者_______后者(填“>”、“<”或“=”)。
(5)氯碱工业是以电解饱和食盐水为基础的基本化学工业。电解饱和食盐水的产物中一种是所有气体中密度最小的气体、一种是黄绿色气体和一种易溶、易电离的碱,则电解食盐水的化学方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积为2 L的密闭容器内加入0.2 mol N2和0.6 mol H2,在一定条件下发生如下反应:N2(g)+3H2(g)![]() 2NH3 ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示:
2NH3 ΔH<0。反应中NH3的物质的量浓度的变化情况如图所示:
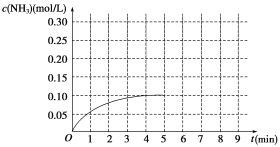
(1)根据图示,计算从反应开始到第4分钟达到平衡时,平均反应速率υ(N2)为__________。
(2)达到平衡后,第5分钟末,若保持其它条件不变,只改变反应温度,则NH3的物质的量浓度不可能为_____________。
a.0.20 mol/L b.0.12 mol/L c.0.10 mol/L d.0.08 mol/L
(3)达到平衡后,第5分钟末,若保持其它条件不变,只把容器的体积缩小,新平衡时NH3的浓度恰好为原来的2倍,则新体积_____(选填“大于”、“等于”、“小于”)二分之一倍的原体积,化学平衡常数________(选填“增大”、“减小”或“不变”)。
(4)在第5分钟末将容器的体积缩小一半,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L)。请在图中画出第5分钟末到达新平衡时NH3浓度的变化曲线_____。
(5)已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com