
【题目】镁和铝的碱式碳酸盐是中和胃酸药物的主要成分。欲测定某种镁和铝的碱式碳酸盐的成分进行了以下实验,根据以下实验记录,回答下列问题:
(1)称取6.02g该碱式碳酸盐,加入4.0mol/L盐酸使其溶解,当加入42.5mL时开始产生CO2,当加入盐酸至45.0mL时恰好完全溶解,该碱式碳酸盐中OH-与CO32- 的物质的量之比n(OH-)︰n(CO32-)=__________;
(2)在上述碱式碳酸盐恰好完全溶解所得溶液中加入过量的NaOH溶液,过滤,干燥(不分解)后得3.48g沉淀物。若该碱式碳酸盐中镁元素与氢元素的质量分数之比为6:1,试计算确定该碱式碳酸盐的化学式 __________________。
【答案】 16:1 Al2Mg6(OH)16(CO3). 4H2O
【解析】(1)当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,可得n(CO2)=n(CO32-)=2.5×10-3×4=0.01mol,而中和OH-需要盐酸42.5-2.5=40mL,所以n(OH-)=40×10-3×4=0.16mol。该碱式碳酸盐中OH-与CO32- 的物质的量之比n(OH-)︰n(CO32-)=0.16mol:0.01mol=16:1;(2)在上述碱式碳酸盐恰好完全溶解所得溶液中加入过量的NaOH溶液,过滤,干燥(不分解)后得3.48g沉淀物。沉淀物为氢氧化镁,则![]() ,根据上述分析可知,
,根据上述分析可知, ![]() ,
, ![]() ,
, ![]() ,根据电荷守恒
,根据电荷守恒![]() ,得
,得![]() ,则碱式碳酸盐的化学式为Al2Mg6(OH)16(CO3)xH2O,若该碱式碳酸盐中镁元素与氢元素的质量分数之比为6:1,则质量比为6:1,则有
,则碱式碳酸盐的化学式为Al2Mg6(OH)16(CO3)xH2O,若该碱式碳酸盐中镁元素与氢元素的质量分数之比为6:1,则质量比为6:1,则有![]() =6,解得x=4,该碱式碳酸盐的化学式Al2Mg6(OH)16(CO3) 4H2O。
=6,解得x=4,该碱式碳酸盐的化学式Al2Mg6(OH)16(CO3) 4H2O。


科目:高中化学 来源: 题型:
【题目】在甲、乙两烧杯溶液中,分别含有大量Cu2+、K+、H+、Cl-、CO32-、OH-6种离子中的3 种,已知甲烧杯的溶液呈碱性,则乙烧杯溶液中大量存在的离子是( )
A. K+、H+、CO32- B. CO32-、OH-、Cl- C. K+、CO32-、Cl- D. Cu2+、H+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质应用的叙述错误的是
A.用Al(OH)3治疗胃酸过多B.用过氧化钠作潜水供氧剂
C.用氧化镁制作耐高温材料D.用氧化铁制作蓝色外墙涂料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 新制氯水可使紫色石蕊试液先变红后褪色
B. 氯水有漂白性是因为HClO的强氧化性
C. 漂白粉是混合物,其有效成分是氯酸钙
D. 新制氯水与久置的氯水中加AgNO3溶液都能生成白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置(电极均为惰性电极)可吸收SO2 , 并用阴极排出的溶液吸收NO2。下列关于该装置的四种说法,正确的组合是( )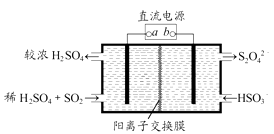
①.a为直流电源的负极
②.阴极的电极反应式为:2HSO3-+2H++2e-=S2O42-+2H2O
③.阳极的电极反应式为:SO2+2H2O-2e-=SO42-+4H+
④.电解时,H+由阴极室通过阳离子交换膜到阳极室
A.①和②
B.①和③
C.②和③
D.③和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于磷酸(H3PO4)的说法中正确的是( )
A.1molH3PO4的质量为98gmol﹣1
B.H3PO4的摩尔质量为98g
C.9.8g H3PO4含有NA个H3PO4分子
D.NA个H3PO4分子的质量为98g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种元素从左向右按原子序数递增(原子序数为5个连续的自然数)的顺序排列如右图所示,下列说法正确的是( ) ![]()
A.E元素的最高化合价为+7价时,D元素的负化合价可为﹣2价
B.A(OH)n为强碱时,B(OH)m也一定为强碱
C.HnDOm为强酸时,E的非金属性一定很强
D.HnCOm为强酸时,E的单质可能有强还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化还原反应的叙述中正确的是( )
A.失去电子的反应为还原反应
B.含有氧元素的物质是氧化剂
C.氧化剂得到电子的数目和还原剂失去的电子的数目一定相等
D.氧化剂和还原剂不可能是同一种物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com