
��ͨ����ִ��ʱ��ʹ�õı�Яʽ�ƾ�����ǿ���Ӧ���ˣ�
3CH3CH2OH+2K2Cr2O7����ɫ��+ 8H2SO4=3CH3COOH +2Cr2(SO4)3������ɫ��+2K2SO4+11H2O��һ��Ӧԭ�������ڸ÷�Ӧ������˵����ȷ���ǣ� ��
A.�÷�Ӧ֤���ˣ������Ԫ�صĻ����һ������ǿ������
B. 1mol��ԭ����Ӧʱ��ת�Ƶĵ�����Ϊ2NA
C. H2SO4�ڷ�Ӧ�б����������Ժ�����
D���������ø÷�Ӧԭ����������Ƴ�ԭ��أ�ͨ��������ǿ���ж�˾���Ƿ�����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�켪��ʡ������ѧ��9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�л�������M�Ľṹ��ʽΪ ���йظû������������ȷ���ǣ� ��
���йظû������������ȷ���ǣ� ��
A�����л������ڷ�����
B�����л��ﲻ������ˮ
C�����л����ԭ��һ������ͬһƽ��
D�����л���ֻ�ܷ����ӳɷ�Ӧ��������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ�ڵ��в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��ɫ��ĩ������������ɣ�Ϊ������ɷֽ�������ʵ�飺��ȡ������Ʒ��������ˮ���в��ֹ���δ�ܽ⣻�ټ�������ϡ���ᣬ�����ݲ���������ȫ���ܽ⣻��ȡ������Ʒ��������ϡ���������ݲ����������й�����ڡ��ð�ɫ��ĩ����Ϊ�� ��
A��NaHCO3��Al(OH)3 B��Na2SO3��BaCO3
C��AgCl��NaHCO3 D��Na2CO3��CuSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�Ƹ��и�����ѧ�ڵ�һ�ε��л�ѧ�Ծ��������棩 ���ͣ������
IBr��ICl��BrF3�ȳ�֮Ϊ±�ػ����(CN)2��(SCN)2����OCN)2�ȳ�֮Ϊ��±�أ����ǵĻ�ѧ���ʾ���±�ص������ƣ���ش��������⡣
��1���Ȼ��⣨ICl���е�Ԫ�صĻ��ϼ�Ϊ____________������ˮ��Ӧ�Ļ�ѧ����ʽΪICl+ H2O= HIO +HCl���÷�Ӧ�ķ�Ӧ����Ϊ___________������ѧ����������Ӧ���ͣ���
��2���廯�⣨IBr������ǿ�����ԣ�����Na2SO3��Һ��Ӧ��������Ӧ�����ӷ���ʽΪ��_______��
��3������֪ijЩ���ӵĻ�ԭ��ǿ��˳��ΪI->SCN->CN->Br->Cl-���ֽ�����KSCN��Һ���뵽������Fe3+����Һ�У���Һ������죬��������ε�������KMnO4��Һ���۲쵽��ɫ����ȥ��������ƽ���ƶ�ԭ��������һ����_______________��
�� ���������У�Ҳ����ʹ����Һ��ɫ��ȥ����_________��
A��������ˮ B.��ˮ C.SO2 D.����
��4��KCNΪ�綾���ʣ���������KCN�ķ�ˮ���õķ����ǣ��ڼ�����������NaClO��Һ��CN-����ΪCO32-��һ�ֵ������壬�÷�Ӧ�����ӷ���ʽΪ__________________��
��5����֪HCN�ĵ���ƽ�ⳣ��K=6.2��10-10��H2CO3�� ����ƽ�ⳣ��K1=4.5��10-7��K2=4.7��10-11�����������ӷ���ʽ�ܷ�������_________��
A.CN-+CO2+H2O=HCN+HCO3- B.2HCN+CO32-=2CN-+CO2��+H2O
C.2CN-+CO2+H2O=HCN+CO32- D.HCN+CO32-=CN-+HCO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�Ƹ��и�����ѧ�ڵ�һ�ε��л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������ʵ��������������ý�����ȷ���ǣ� ��
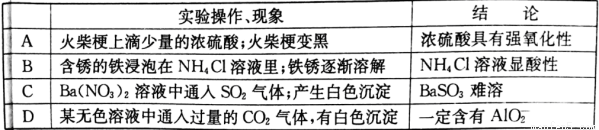
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�Ƹ��и�����ѧ�ڵ�һ�ε��л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ����ȷ���ǣ� ��
A.��Cu��������ⱥ��ʳ��ˮ��Cu+2H+ Cu2++H2��
Cu2++H2��
B.Fe3O4�����������Һ�У�Fe3O4+ 8H++2I-��3Fe2++I2+4H2O
C. NH4Al(SO4)2���ڹ�����ŨBa(OH)2��Һ�� ��
NH4+��A13++2SO42-��2Ba2++5OH-=2BaSO4��+AlO2-+NH3��+H2O
D.����ʯ��ˮ�г��������SO2:SO2+OH-=HSO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ��9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
25 ��ʱ������Ũ�Ⱦ�Ϊ0.2 mol/L��Na2CO3��NaHCO3��Һ��˵������ȷ����( )
A������Һ�о����ڵ���ƽ���ˮ��ƽ��
B������Һ�ֱ��ˮϡ�ͺ�pH��KW����С
C������Һ�о�����c(OH��)��2c(CO32��)��c(HCO3��)��c(Na��)��c(H��)
D��c(OH��)ǰ�ߴ��ں���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ������ѧ��9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ�������ȫ��ȷ����
��� | ʵ�� | ���� |
A | ����ˮ��Ӧ | �����Ӵ�ú����ȡ�������ƣ������̶���С���ƣ�С�ķ���װ��ˮ���ձ��� |
B | ����һ��Ũ�ȵ��Ȼ�����Һ1000mL | ȷ��ȡ�Ȼ��ع��壬���뵽1000ml������ƿ�У���ˮ�ܽ⣬��ҡ�ȣ����� |
C | �ų���ʽ�ζ��ܼ��첿�ֵ����� | ����������ʹ��������б���ϣ�����ָ��ס���ܣ����ἷѹ�����飬ʹ��Һ�Ӽ������� |
D | ȡ����Һ©����������ϲ�Һ�� | �²�Һ��ӷ�Һ©���¶˹ܿڷų����رջ�������һ�������������ϲ�Һ������ӷ�Һ©���¶˹ܿڷų� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij10% NaOH��Һ������������100gˮ��õ�80mL 20%����Һ�����20% NaOH��Һ�����ʵ���Ũ��Ϊ ( )
A��6.25mol��L��1 B��12.5mol��L��1 C��7mol��L��1 D��7.5mol��L��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com