

请回答:
(1)由两种元素形成的化合物溶于水后,溶液中溶质仍然是该化合物,则该化合物所属类别可能为(选择A、B、C、D填空)________;
A.非金属氢化物 B.碱 C.盐 D.氧化物
(2)A元素是________,B元素是________;
(3)若将F溶液在空气中蒸干、灼烧所得产物的化学式为:________________。
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市通州区高三年级上学期期末摸底考试理综化学试卷(解析版) 题型:填空题
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图的转化关系,已知C为密度最小的气体,甲为非电解质。

根据以上转化关系回答下列问题:
(1)写出下列物质的化学式:A B 丁 。
(2)元素A在周期表中的位置是 ,写出甲的一 种用途 。
(3)写出下列变化的方程式:
A与NaOH溶液反应的化学方程式
乙与过量CO2反应的离子方程式
查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁省五校协作体高三冲刺最后一模化学试卷(解析版) 题型:推断题
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图的转化关系,已知C为密度最小的气体,甲为非电解质。
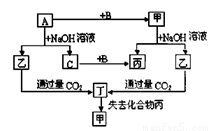
根据以上转化关系回答下列问题:
(1)写出下列物质的化学式:A B 丁 。
(2)元素A在周期表中的位置是 ,写出甲的一种用 途 。
(3)写出下列变化的方程式:
A与NaOH溶液反应的化学方程式 。
乙与过量CO2反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:陕西省模拟题 题型:填空题
 CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95×1011  CH3CH2OH(g)+H2O(g) 25℃时,K=1.71×1022
CH3CH2OH(g)+H2O(g) 25℃时,K=1.71×1022 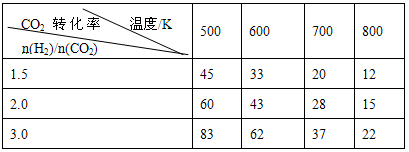
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com