
【题目】下列有关焰色反应的说法错误的是( )
A.观察K2SO4的焰色应透过蓝色的钴玻璃
B.Na与NaCl在灼烧时火焰颜色相同
C.可以用焰色反应来区别NaCl和KCl
D.焰色反应一定发生化学变化
科目:高中化学 来源: 题型:
【题目】选择下列实验方法分离物质,将分离方法的序号填在横线上. A.萃取分液 B.升华 C.结晶 D.分液 E.蒸馏 F.过滤
(1)分离粗盐中混有的泥沙 .
(2)分离碘和水的混合物 .
(3)分离水和汽油的混合物
(4)分离酒精和水的混合物 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学在日常生活中用途广泛,下图①是镁、次氯酸钠燃料电池的示意图,电池总反应式为:Mg+ClO-+H2O═Cl-+Mg(OH)2↓,图②是电解法除去工业废水中的Cr2O72-.下列说法正确的是
A. 图②中Cr2O72-离子向铁电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
B. 图②中阳极上的电极反应式为:Fe-3e-═Fe3+
C. 图①中发生的氧化反应是:ClO-+H2O+2e-═Cl-+2(OH)-
D. 若图①中7.2g镁溶解产生的电量用以图②废水处理,理论可除去Cr2O72-的物质的量为0.05mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PCl3有毒,在潮湿的空气中可发生水解反应产生大量的白雾。它在实验室和工业上都有重要的应用。在实验室中制取PCl3,在D中放入足量白磷,将Cl2迅速而且不间断地通入D中,氯气与白磷会发生反应,产生火焰。

三氯化磷和五氯化磷的物理常数如下:
熔点 | 沸点 | |
三氯化磷 | -112℃ | 76℃ |
五氯化磷 | 146℃ | 200℃分解 |
注:常温下五氯化磷不溶于三氯化磷
(1)写出A中发生反应的化学方程式:____________________________。
(2)反应开始前需要检查装置气密性,检查方法为____________________________。
(3)氯气和白磷反应放出大量的热,为使仪器D不致因局部过热而炸裂,实验开始前应在D的底部放少量____________________________。
(4)在烧杯E中加入冰盐水,其作用是____________________________。
(5)白磷与氯气反应产物中可能含有一定量的PCl5,从中分离出三氯化磷的方法是______________。经过一段时间反应发现B中竖直导管液面上开,可能的原因是____________________________。
(6)装置F的作用是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10 mol·L-1NaOH 溶液分别滴定20.00mL 浓度均为0.10 mol·L-1CH3COOH溶液和HCN溶液所得滴定曲线如右图。下列说法正确的是

A. 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B. 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
C. 点③和点④所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D. 点①和点②所示溶液中:c(CH3COO-)<c(CN-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释 100 倍(体积之比)后使用。请回答下列问题:

(1)该“84消毒液”的物质的量浓度约为________ mol·L1(计算结果保留 2位有效数字)。
(2)某同学取 100mL 该“84消毒液”,稀释后用于消毒,稀释后的溶液中 c(Na+)=_______ mol·L1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制 480mL含NaClO质量分数为25%的消毒液。下列说法正确的是______(填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B. 将称量好的NaClO固体在烧杯中溶解后应立即转入容量瓶并加水至刻度线
C. 定容时俯视容量瓶刻度线会导致所配溶液浓度偏高
D.需要称量 NaClO固体的质量为 143.0g

(4)该同学对容量瓶及其使用方法的认识中正确的是________
A.容量瓶上标有容积、温度和浓度
B.容量瓶用蒸馏水洗净后, 需要烘干后再使用
C.配制溶液过程中,容量瓶内液体只需要一次摇匀过程
D.使用前要检查容量瓶是否漏水
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用 98%(密度为1.84g·cm3)的浓硫酸配制 2L 2.3mol·L1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为_______ mol·L1。
②需用浓硫酸的体积为_______mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学一-有机化学基础]在碱的作用下,两分子酯缩合形成β一羰基酯,同时失去一分子醇,该反应称克莱(R·L·Claisen)酯缩合反应,其反应机理如下: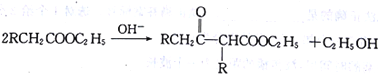 。利用Claisen反应制备化合物H的一种合成路线如下:
。利用Claisen反应制备化合物H的一种合成路线如下:
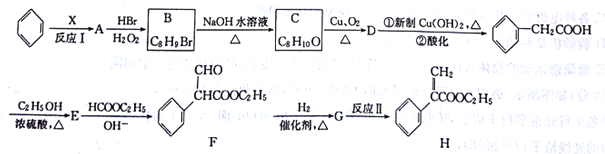
回答下列问题:
(1)反应Ⅰ的反应物和生成物的实验式均相同,则X的结构简式为_____,A的名称为____。
(2)F中含氟官能团的名称是_______;反应Ⅱ的反应类型是________。
(3)E![]() F反应的化学方程式为________。
F反应的化学方程式为________。
(4)B的含有苯环的同分异构体有____种(B自身除外),其中核磁共振氢谱显示3组峰的结构简式为__________、_________。
(5)乙酰乙酸乙酯是一种重要的有机合成原料,写出由乙醇制备乙酰乙酸乙酯的合成路线___________(无机试剂任进)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室可用如图所示装置制取少量乙酸乙酯。有关叙述不正确的是( )

A. 长导管起冷凝、导气的作用
B. 用蒸馏法从所得混合溶液中分离出乙酸乙酯
C. Na2CO3饱和溶液的作用之一是吸收未反应的乙酸
D. 导管末端不插入饱和Na2CO3溶液中是为了防倒吸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com