
| A、在某试液中滴加BaCl2溶液得白色沉淀,取该白色沉淀加稀硝酸不溶解,则原未知试液中一定含有S042- |
| B、在某试液中滴加NaOH溶液得白色沉淀,继续滴加该白色沉淀溶解,则原未知试液中一定含有Al3+ |
| C、在未知试液中滴加盐酸产生无色气体,将该气体通入过量澄清石灰水中得白色沉淀,则原未知试液中一定含有C032- |
| D、某未知气体通入品红溶液中,品红溶液褪色,则原气体一定是S02 |


科目:高中化学 来源: 题型:
| 高温 |
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
查看答案和解析>>
科目:高中化学 来源: 题型:
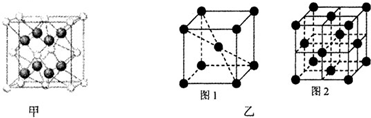
| 元素 | 结构或性质信息 |
| A | 原子核外有一个未成对电子,其氢化物与水分子间能形成氢键 |
| B | 原子核外M层电子数是N层电子数的4倍 |
| C | 是使用最为广泛的合金的主要成分 |
| D | 原子各内层电子均已饱和,最外层电子数为1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不可将温度计当搅拌棒使用,也不可靠在容器内壁上 |
| B、搅拌时,环形玻璃搅拌棒应上下移动 |
| C、测量反应混合液的温度时要随时读取温度,记录下最高温度 |
| D、为了使反应完全,必须保证酸和碱恰好完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
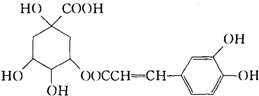 咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示:1mol咖啡鞣酸与NaOH完全反应时可消耗 NaOH物质的量是( )
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示:1mol咖啡鞣酸与NaOH完全反应时可消耗 NaOH物质的量是( )| A、2 molNaOH |
| B、4 molNaOH |
| C、6 molNaOH |
| D、8 molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.6a g |
| B、(a-1.6)g |
| C、(a-3.2)g |
| D、1.6 g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下0.1 mol/L的下列溶液①NH4Al(SO4)2②NH3?H2O③NH4Cl ④CH3COONH4中,c(NH4+)由大到小的顺序是:①>③>④>② |
| B、常温时,pH=2的CH3COOH溶液和pH=12的氨水等体积混合;pH=2的HCl溶液和pH=12的NaOH溶液等体积混合,各混合溶液中由水电离的c(H+)一定相等 |
| C、常温下0.4mol/L HB溶液和0.2mol/L NaOH溶液等体积混合后,则混合后溶液中离子浓度的大小顺序一定为:c(B-)>c(Na+)>c(H+)>c(OH-) |
| D、0.lmol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N元素的电负性较大,但N2的化学性质很稳定 |
| B、F2比O2更容易与H2反应 |
| C、HF、HCl、HBr、HI的稳定性逐渐减弱 |
| D、稀有气体一般难发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com