
 +2NaOH
+2NaOH| 水 |
| △ |
 +2NaCl
+2NaCl +2NaOH
+2NaOH| 水 |
| △ |
 +2NaCl
+2NaCl +O2
+O2| 催化剂 |
| △ |

 +O2
+O2| 催化剂 |
| △ |

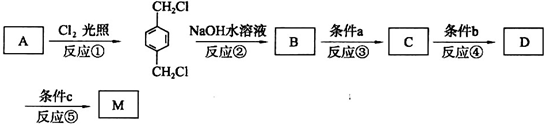
 .A与氯气在光照的条件下发生取代反应生成
.A与氯气在光照的条件下发生取代反应生成 ,故A为
,故A为 ,
, 在NaOH水溶液条件下生成水解反应生成B,B为
在NaOH水溶液条件下生成水解反应生成B,B为 ,B在金属铜或银作催化剂、加热条件下,被氧气氧化性生成C为
,B在金属铜或银作催化剂、加热条件下,被氧气氧化性生成C为 ,进一步发生氧化反应生成D,D发生酯化反应生成对苯二甲酸酯M,据此解答.
,进一步发生氧化反应生成D,D发生酯化反应生成对苯二甲酸酯M,据此解答. .A与氯气在光照的条件下发生取代反应生成
.A与氯气在光照的条件下发生取代反应生成 ,故A为
,故A为 ,
, 在NaOH水溶液条件下生成水解反应生成B,B为
在NaOH水溶液条件下生成水解反应生成B,B为 ,B在金属铜或银作催化剂、加热条件下,被氧气氧化性生成C为
,B在金属铜或银作催化剂、加热条件下,被氧气氧化性生成C为 ,进一步发生氧化反应生成D,D发生酯化反应生成对苯二甲酸酯M,
,进一步发生氧化反应生成D,D发生酯化反应生成对苯二甲酸酯M, 有多种同分异构体,其中含有苯环且只有一个支链的同分异构体,则支链为乙基,该同分异构体为
有多种同分异构体,其中含有苯环且只有一个支链的同分异构体,则支链为乙基,该同分异构体为 ,名称是乙苯,
,名称是乙苯, 发生酯化反应生成对苯二甲酸酯M,
发生酯化反应生成对苯二甲酸酯M, 在金属铜或银作催化剂、加热条件下,被氧气氧化性生成
在金属铜或银作催化剂、加热条件下,被氧气氧化性生成 ,
, 在NaOH水溶液条件下生成水解反应生成
在NaOH水溶液条件下生成水解反应生成 ,反应方程式为:
,反应方程式为: +2NaOH
+2NaOH| 水 |
| △ |
 +2NaCl,
+2NaCl, 在一定条件下氧化生成
在一定条件下氧化生成 ,反应方程式为:
,反应方程式为: +O2
+O2| 催化剂 |
| △ |
 ,
, +2NaOH
+2NaOH| 水 |
| △ |
 +2NaCl;
+2NaCl; +O2
+O2| 催化剂 |
| △ |
 .
.

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| O | 2- 3 |
| O | 2- 4 |
| O | 2- 4 |
| O | 2- 4 |
| O | - 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
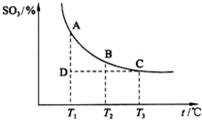 (2013?潍坊模拟)如图,研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义.
(2013?潍坊模拟)如图,研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义.| 3 |
| 2 |
| H | 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com