
能说明M的非金属性比N强的事实是
| A.M的气态氢化物比N的气态氢化物稳定 |
| B.HxM的酸性比HyN的酸性强 |
| C.单质M的熔沸点比单质N的溶沸点高 |
| D.M能将N从它的盐溶液中置换出来 |
科目:高中化学 来源: 题型:填空题
(1)某建筑材料,主要成分为铝硅酸盐,化学式是MgAl2H4Si4O14;化学式改写成氧化物形式为_________。该材料与酸或碱反应时可以看作各氧化物分别与酸、碱反应,则材料该与足量的氢氧化钠反应后过滤,滤渣主要是_______。
(2)除去FeCl2溶液中少量的FeCl3最好加入_________物质。
(3)鉴别Na2CO3和NaHCO3溶液可选用_________。(填序号)
①NaOH;②Ca(OH)2;③BaCl2;④K2SO4;⑤Ca(NO3)2
(4)某溶液中有①SO42―②Mg2+③Fe2+④Al3+四种离子,若向其中加入过量的氢氧化钠溶液,加热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
(5)将盛有18mLNO2和O2的混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积是( )
①1.2mL②2.4mL③3.6mL④5.2mL
| A.①② | B.①③ | C.②④ | D.①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图为部分短周期元素化合价与原子序数的关系图。请回答下列问题。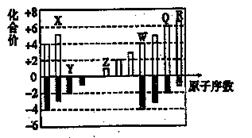
(1)元素Q位于周期表中第 周期______族。
(2)将X、Z、Q、R四种元素的氢化物各1mol和水混合后,分剜得到l L溶液,所得水溶液碱性最强的氢化物的电子式是 。
(3)Z的最高价氧化物对应的水化物与W的单质反应的化学方程式为 。
(4)水中锰含量超标,容易使洁具和衣物染色、使水产生异味。RY2可以用来除去水中超标的Mn2+,生成一种黑色沉淀,同时测得消耗13.50 g RY2时,共转移了1 mol电子。则反应的离子方程式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于F、Cl、Br、I的比较,说法正确的是
| A.原子最外层的电子数随核电荷数的增加而增多 |
| B.简单阴离子的还原性随核电荷数的增加而增强 |
| C.氢化物的稳定性随核电荷数的增加而增强 |
| D.非金属性随核电荷数的增加而增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X?Y?Z的原子序数依次增大,Y为IA族元素,X与Z同主族,3种元素原子的最外层电子数之和为13?下列判断正确的是
| A.Y元素位于第2周期 | B.Y?Z均能与X形成不只一种化合物 |
| C.X是ⅤA族元素 | D.氢化物的稳定性:HnZ>HnX |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +3、+5、-3 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z均为短周期元素,在周期表中的位置如下图所示,下列叙述正确的是
| | | Z |
| | Y | |
| X | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com