
【题目】下列反应中,生成物的总能量大于反应物总能量的是( )
A.氢气在氧气中燃烧B.锌和稀硫酸反应制取氢气
C.氧化钙和水的反应D.焦炭在高温下与水蒸气反应
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某研究性小组决定用实验探究的方法证明化学反应具有一定的限度。取5mL 0.1mol/L KI溶液于试管中,滴加0.1mol/L FeCl3溶液2mL,发生如下反应:2Fe3++2I-![]() 2Fe2++I2。为证明该反应具有可逆性且具有限度,他们设计了如下实验:
2Fe2++I2。为证明该反应具有可逆性且具有限度,他们设计了如下实验:
①取少量反应液,滴加AgNO3溶液,发现有少量黄色沉淀(AgI),证明反应物没有反应完全;
②再取少量反应液,加入少量CCl4,振荡,发现CCl4层显浅紫色,证明萃取到I2,即有I2生成。综合①②的结论,他们得出该反应具有一定的可逆性,在一定条件下会达到反应限度。
(1)老师指出他们上述实验中①不合理,你认为是_____________________________;在不改变反应物用量的前提下,改进的方法是_____________________________________________。
(2)有人认为步骤②适合检验生成I2较多的情况下,还有一种简便方法可以灵敏地检验是否生成了I2,这种方法是______________________________。
(3)控制适合的条件,将反应2Fe3++2I-![]() 2Fe2++I2,设计成如图所示的原电池。
2Fe2++I2,设计成如图所示的原电池。

①反应开始时,乙中石墨电极上发生____________(填“氧化”或“还原”)反应,电极反应式为_________________________。
②电流计读数为0时,反应达到平衡状态。此时在甲中加入FeCl2固体,发现电流计又发生偏转,则甲中的石墨作_______(填“正”或“负”)极,该电极的电极反应式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中:2A(g)+B(g)![]() 2C(g)+D(g),若最初加入的A和B都是4mol,在前10s A的平均反应速率为0.12mol/(L·s),则10s时,容器中B的物质的量是( )
2C(g)+D(g),若最初加入的A和B都是4mol,在前10s A的平均反应速率为0.12mol/(L·s),则10s时,容器中B的物质的量是( )
A. 3.4 mol B. 3.2 mol C. 2.8 mol D. 1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[物质结构与性质]
根据物质结构有关性质和特点,回答下列问题:
(1)Ti基态原子核外电子排布式为__________,基态铝原子核外电子云形状有_______(填形状名称)
(2)丙烯腈(CH2=CH-CN)分子中σ键和π键的个数比为_______,分子中碳原子轨道的杂化类型是________。
(3)写出与NH4+互为等电子体的一种分子和一种离子的化学式________、_______。
(4)钛存在两种同素异构体,α-Ti为六方最密堆积,β-Ti为体心立方堆积,鉴别两种钛晶体可以用_______法,由α-Ti转变为β-Ti晶体体积_________(填“膨胀”或“收缩”)。
(5)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_________形象化描述。
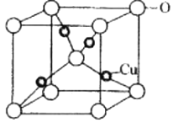
(6)Cu与O元素形成的某种化合物的晶胞结构如图所示,晶胞中氧原子的配位数为_________,若阿伏加德罗常数为NA,晶胞的边长为apm,该晶体的密度为_________g·cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人造地球卫星用到的一种高能电池--银锌蓄电池,其电池的电极反应式为:2Zn+2OH--2e-===2ZnO+H2↑,Ag2O+H2O+2e === 2Ag+2OH- 。据此判断锌是( )
A.负极,并被氧化B.正极,并被还原
C.负极,并被还原D.正极,并被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是一种常见金属,F是一种红褐色沉淀。试根据图中转化关系,回答下列问题。

(1)A的原子序数为26,A元素在周期表中的位置:______,写出NaOH 的电子式:_____。
(2)写出检验D中阳离子的操作方法为_________________________。
(3)保存C溶液时要加固体A的原因是______________。
(4)写出下列转化的方程式:
①B→C的离子方程式:______________________________。
②E→F的化学方程式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法中,不正确的是( )
A.Al2O3做耐火坩埚
B.Fe3O4用作红色油漆和涂料
C.NaHCO3用于蒸馒头
D.Na2O2用作供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在5L的密闭容器中进行以下反应:4NH3+5O2=4NO+6H2O,半分钟后冷却至室温,测得NO的物质的量增加了0.3mol,则此反应的平均反应速率υ(X)为( )
A. υ(H2O)=0.12mol·L-1·min-1B. υ(O2)=0.30mol·L-1·min-1
C. υ(NO)=0.008mol·L-1·s-1D. υ(NH3)=0.002mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com