
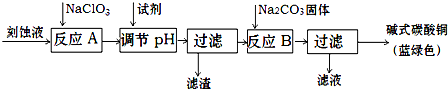
| 物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |


科目:高中化学 来源: 题型:
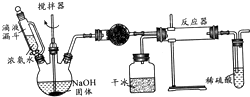 实验室制备氨基甲酸铵(NH2COONH4)的反应如下:2NH3(g)+CO2(g)?NH2COONH4(s),该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵.
实验室制备氨基甲酸铵(NH2COONH4)的反应如下:2NH3(g)+CO2(g)?NH2COONH4(s),该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
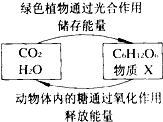 如图是两组物质之间在一定的条件下相互转化的过程.下列绿色植物通过光合作用说法不正确的是( )
如图是两组物质之间在一定的条件下相互转化的过程.下列绿色植物通过光合作用说法不正确的是( )| A、物质X是O2 |
| B、绿色植物通过光合作用,将太阳能转化成化学能 |
| C、C6H12O6是碳氢氧三种元素组成的化合物 |
| D、C6H12O6与X反应生成CO2和H2O属于置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
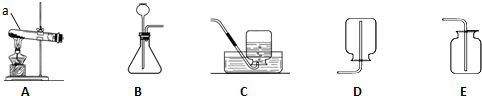
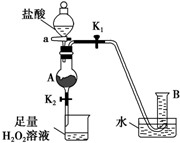 如图装置(夹持装置略,气密性已检验)某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体,下列推断不合理的是( )
如图装置(夹持装置略,气密性已检验)某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体,下列推断不合理的是( )| A、B中收集到的气体是氢气 |
| B、烧杯中双氧水溶液作用是将Fe2+还原为Fe3+ |
| C、A中的氧化铁与盐酸反应生成氯化铁 |
| D、烧杯中溶液在氯化氢气氛下,蒸发浓缩、冷却结晶、过滤后得到氯化铁晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用丙酮与盐酸的混合液作展开剂,对Fe3+与Cu2+用纸层析法分离时,Fe3+移动较快 |
| B、阿司匹林制备实验中,将粗产品加入饱和NaOH溶液中以除去水杨酸聚合物 |
| C、用瓷坩锅高温熔融NaOH和Na2CO3的固体混合物 |
| D、标准盐酸滴定待测NaOH溶液,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg、NO2、O2 |
| B、MgO、NO2、O2 |
| C、Mg3N2、O2 |
| D、MgO、NO2、N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
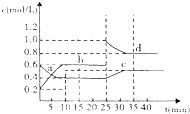 已知A与B相互转化:2A(g)?B(g);△H=-24.4J/mol.在恒温下,将一定量的A和B混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图,下列推断合理的是( )
已知A与B相互转化:2A(g)?B(g);△H=-24.4J/mol.在恒温下,将一定量的A和B混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图,下列推断合理的是( )| A、前10min内,用v(A)为0.02mol/(L?min) |
| B、反应进行前10min时,体系吸收热量9.76kJ |
| C、b、c、d三点中反应速率d>b=c |
| D、25min时,导致平衡移动的原因是升温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
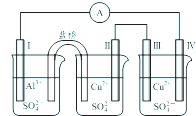 某同学组装了如图所示的电化学装置,电极Ⅰ为Al电极,其它均为Cu电极,则下列叙述正确的是( )
某同学组装了如图所示的电化学装置,电极Ⅰ为Al电极,其它均为Cu电极,则下列叙述正确的是( )| A、电子流动方向:电极Ⅳ→A→电极Ⅰ |
| B、电极Ⅰ发生氧化反应 |
| C、电极Ⅱ质量不变 |
| D、电极Ⅲ的电极反应:Cu2++2e-=Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com