
| A. | 熔点:纯铁>生铁 | B. | 密度:硝基苯>水 | ||
| C. | 热稳定性:小苏打<苏打 | D. | 碳碳键键长:乙烯>苯 |
分析 A.生铁是合金,合金的熔点一般小于各组分的熔点;
B.水的密度等于1g/ml,硝基苯的密度大于1g/ml;
C.碳酸氢钠不稳定受热分解生成碳酸钠;
D.苯中碳碳键介于单键和双键之间.
解答 解:A.生铁是合金,熔点小于纯铁的熔点,故熔点为纯铁>生铁,故A正确;
B.水的密度等于1g/ml,硝基苯的密度大于1g/ml,所以密度:水<硝基苯,故B正确;
C.碳酸氢钠不稳定受热分解生成碳酸钠,所以热稳定性:NaHCO3<Na2CO3,故C正确;
D.苯中碳碳键介于单键和双键之间,碳碳键键长:乙烯<苯,故D错误.
故选D.
点评 本题考查元素及其对应单质、化合物的性质的递变规律,侧重于熔点、热稳定性、密度等性质的考查,题目难度不大,注意把握性质比较的角度以及规律.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用乙二醇的物理性质作内燃机抗冻剂 | |
| B. | 煤经过气化和液化两个物理变化,可变为清洁能源 | |
| C. | 采用光触媒技术可将汽车尾气中的NO和CO转化为无毒气体 | |
| D. | 苦卤经过浓缩、氧化、鼓入热空气或水蒸气,可获得溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分离苯和硝基苯:蒸馏 | B. | 分离氯化钠与氯化铵固体:升华 | ||
| C. | 分离水和溴乙烷:分液 | D. | 分离氯化钠和硝酸钾:结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物的总键能低于生成物的总键能 | |
| B. | 1mol I2(g)中通入1mol H2(g),反应放热11kJ | |
| C. | 等物质的量时,I2(g)具有的能量低于I2(l) | |
| D. | 平衡时分离出HI(g),正反应速率先减小后增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO的结构式:H-O-Cl | B. | HF的电子式: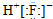 | ||
| C. | S2-的结构示意图: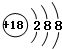 | D. | CCl4分子的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2作为反应物,转移电子数一定为2NA | |
| B. | 1molC9H20中含有共价键数目为28NA | |
| C. | 标况下448mL二氯甲烷中含有分子数为0.02NA | |
| D. | 常温常压下,1.8 g重水(D2O)中含中子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(K+)=c(HC2O4-)+c(H2C2O4)+2c(C2O42-) | B. | c(Na+)=c(H2C2O4)+c(C2O42-) | ||
| C. | c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-) | D. | c(K+)>c(Na+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com