
烧瓶中放入铜片和稀硝酸,来制取较纯净的一氧化氮,反应开始后发现烧瓶中出现红棕色气体,这时的操作应是( )
A.立即接上收集容器,用向上排空气法收集
B.待烧瓶中红棕色气体消失后,用向上排空气法收集
C.待烧瓶中红棕色气体消失后,用排水法收集
D.立即用排水法收集
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
2K3[Fe(C2O4)3]═3K2CO3+Fe+FeO+4CO↑+5CO2↑元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值。
(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉作显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰。相关的反应如下:
4FeCl3+2NH2OH•HCl= 4FeCl2+N2O↑+6HCl+H2O
①Fe3+在基态时,核外电子排布式 ls22s22p63s23p63d6或[Ar]3d6 ;
②羟胺中(NH2OH)采用sp3杂化的原子有N、O ,三种元素电负性由大到小的顺
序为 ;
③Fe2+与邻啡罗啉(用A表示)形成的配合物[FeA3] 2+中,Fe2+的配位数为 6 ;
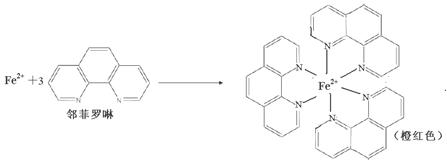
④N2O分子的空间构型为 (用文字描述)。
 (2)分子氢的规模化制备是氢能应用的基础。在光化学电池中,以紫外线照钛酸锶电极时,可
(2)分子氢的规模化制备是氢能应用的基础。在光化学电池中,以紫外线照钛酸锶电极时,可
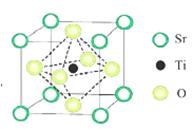
分解水制取H2同时获得O2。已知钛酸锶晶胞结构如
图所示,则钛酸锶的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
当我们看电视、阅读报刊或浏览网站时,经常可以看到一些城市的空气质量报告,影响空气质量的一组主要污染物是( )
A.SO2 NO2 可吸入颗粒物
B.CO2 N2 O2
C.CO2 O2 SO2
D.NO2 N2 可吸入颗粒物
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸、硝酸与盐酸是工业上常用的三大强酸。工业上制备硫酸常用接触法,工业上制硝酸是用氨的催化氧化法。下列关于工业上制硫酸与硝酸的说法中不正确的是( )
A.在沸腾炉中进行的反应为:4FeS2+11O2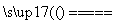 2Fe2O3+8SO2
2Fe2O3+8SO2
B.氨被氧气催化氧化:4NH3+5O2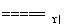 4NO+6H2O
4NO+6H2O
C.硫酸工业、硝酸工业都需要对工业尾气进行处理
D.接触法制硫酸的原料为:二氧化硫、空气、水
查看答案和解析>>
科目:高中化学 来源: 题型:
三位学生设计了下述三个方案,并都认为,如果观察到的现象和自己设计的方案一致,即可确认试液中含有SO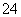 。
。
方案甲:试液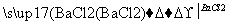 白色沉淀
白色沉淀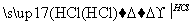 沉淀不溶解
沉淀不溶解
方案乙:试液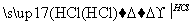 无沉淀
无沉淀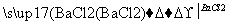 白色沉淀
白色沉淀
方案丙:试液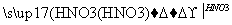 无沉淀
无沉淀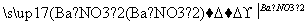 白色沉淀
白色沉淀
试评价上述各种方案是否严密,并分别说明理由。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知标准状况下:①6.72L CH4②3.01×1023HCl ③23.1g CCl4④2.3g Na,下列对四种物质的关系由小到大表示正确的是( )
|
| A. | 体积 ④<①<②<③ | B. | 密度 ①<④<③<② |
|
| C. | 原子数 ④<③<②<① | D. | 质量 ④<①<③<② |
查看答案和解析>>
科目:高中化学 来源: 题型:
银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下:

(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450 ℃和80 ℃)
(1)电解精炼银时,阴极反应式为__________________;滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学反应方程式为________________________________________________________ ________________________________________________________________________________________。
(2)固体混合物B的组成为________;在生成固体B的过程中,需控制NaOH的加入量。若NaOH过量,则因过量引起的反应的离子方程式为________________________________________________________________________。
(3)完成煅烧过程中一个反应的化学方程式:________CuO+______Al2O3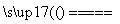 ______CuAlO2+______↑。
______CuAlO2+______↑。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0 kg废料中的铜可完全转化为________mol CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液________L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是________、过滤、洗涤和干燥。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com