
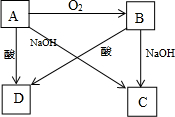
分析 (1)A是一种常见非金属,且是一种半导体材料,应为Si,由转化关系可知B为SiO2,C为Na2SiO3,D应为SiF4;
(2)A是一种常见金属,既可与酸反应,也可与碱反应,则应为Al,由转化关系可知B为Al2O3,C为NaAlO2,D含有Al3+.
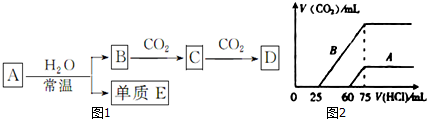
解答 (1)A是一种常见非金属,且是一种半导体材料,应为Si,由转化关系可知B为SiO2,C为Na2SiO3,D应为SiF4,
①B为SiO2,可与HF酸反应,反应的化学方程式为SiO2+4HF=2H2O+SiH4↑,故答案为:SiO2+4HF=2H2O+SiH4↑;
②Ai可与NaOH溶液反应,反应的离子方程式为Si+2OH-+H2O=SiO32-+2H2↑,故答案为:Si+2OH-+H2O=SiO32-+2H2↑;
(2)A是一种常见金属,既可与酸反应,也可与碱反应,则应为Al,由转化关系可知B为Al2O3,C为NaAlO2,D含有Al3+.
①Al与非氧化性酸反应生成Al3+和氢气,反应的离子方程式为2Al+6H+=2Al3++3H2↑,
故答案为:2Al+6H+=2Al3++3H2↑;
②B为Al2O3,C为NaAlO2,B可与氢氧化钠溶液反应生成C,反应的化学方程式为Al2O3+2NaOH=NaAlO2+2H2O,
故答案为:Al2O3+2NaOH=NaAlO2+2H2O.
点评 本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握A连续与X反应的特点,为解答该题的突破口,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石墨与O2反应 | B. | 硫磺与O2反应 | ||
| C. | 闪电时,氮气与O2反应 | D. | 硅在足量的O2中燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2溶液与Na2S03溶液加足量稀HNO3 | |
| B. | Ba(0H)2溶液与KN03溶液加足量稀H2SO4 | |
| C. | AgN03溶液与Na2C03溶液加足量稀盐酸 | |
| D. | Ca(0H)2溶液与FeCl3溶液加足量稀HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 42.0g | B. | 21.3g | C. | 7.1g | D. | 3.55g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向亚磷酸溶液中加入过量的烧碱溶液(亚磷酸是二元弱酸):H3PO3+3OH-═PO33-+3H2O | |
| B. | 2mol•L-1的AlCl3溶液和7mol•L-1的NaOH溶液等体积混合:2Al3++7OH-═Al(OH)3↓+AlO${\;}_{2}^{-}$+2H2O | |
| C. | 用硝酸酸化的硝酸铁溶液可以刻蚀银饰:Fe3++Ag═Fe2++Ag+ | |
| D. | H218O中投入Na2O2固体:2H218O+2Na2O2═4Na++4OH-+18O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com