
由下列反应式所得出的结论中正确的是
A.HClO+SO2+H2O=HCl+H2SO4:酸性 HClO>H2SO4
B.Al2O3+2NaOH=2NaAlO2+H2O:Al2O3是两性氧化物
C.NH3+H3O+=NH4++H2O:NH3结合H+的能力比H2O强
D.已知C(s,石墨)=C(s,金刚石) ΔH=+1.9 kJ/mol:金刚石比石墨稳定
科目:高中化学 来源:2016届安徽省江南十校新高三摸底联考化学试卷(解析版) 题型:实验题
(12分)铝热反应是铝的一个重要性质。某校化学兴趣小组同学为了克服传统铝热反应纸漏
斗易燃烧,火星四射等缺点,将实验改成以下装置,取磁性氧化铁在如图A实验进行铝热反应,冷却后得到“铁块”混合物.

(1)实验中可以用蔗糖和浓硫酸代替镁条作引火剂,共原因是 。
(2)该铝热反应的化学方程式为 。
(3)取反应后的“铁块”研碎取样称量,加入如图B装置,滴入足量NaOH溶液充分反应,测量生成气体体积以测量样品中残留铝的百分含量.试回答下列问题:
①量气管的量具部分是一个中学实验常见量具改装而成,该仪器的名称为
②量气管在读数时必须进行的步骤是 。
③取1g样品进行上述实验,共收集到44.8mL气体(换算成标准状况下),则铝的百分含量为 。
④装置中分液漏斗上端和试管用橡胶管连通,除了可以平衡压强让液体顺利滴入试管之外,还可以起到降低实验误差的作用。如果装置没有橡胶管,测出铝的百分含量将会 填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一入学摸底化学试卷(解析版) 题型:填空题
(8分)有一包白色固体混合物,该混合物可能含有CuSO4、Na2CO3、Na2SO4、MgCl2,现进行如下实验:
(1)将混合物溶于水,得到无色透明溶液。
(2)取上述溶液分成两份盛于试管中,其中一份滴加BaCl2溶液,产生白色沉淀,再加稀硝酸,沉淀不溶解;另一份滴加NaOH溶液,有白色沉淀生成。试根据实验现象推断,并完成下面的填空:
该混合物中肯定没有________和________;肯定含有________和________(写化学式)。
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三9月月考化学试卷(解析版) 题型:实验题
(14分)铜在自然界存在于多种矿石中.
(Ⅰ)以硅孔雀石(主要成 分为CuSiO3•2H2O,含少量SiO2、FeCO3、Fe2O3等杂质)为原料制取硫酸铜的工艺流程如下:
分为CuSiO3•2H2O,含少量SiO2、FeCO3、Fe2O3等杂质)为原料制取硫酸铜的工艺流程如下:
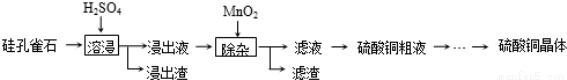
已知:Fe3+、Cu2+和Fe2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、6.7和9.7.
(1)“溶浸”中CuSiO3•2H2O和H2SO4发生反应的化学方程式 .
(2)“溶浸”中,选取浓度为20% H2SO4为浸出剂,铜的浸出率与浸出时间的关系见图1.由图1可得,随着浸出时间的增长, (至少写一条变化规律).

(3)“除杂”中,加入MnO2的作用是 (用离子方程式表示).“除杂”中需在搅拌下加入石灰乳以调节溶液的pH到3~4,沉淀部分杂质离子,分离得滤液.滤渣的主要成分为 .
(Ⅱ)以黄铜矿(主要成分为CuFeS2)为原料炼制精铜的工艺流程如下:
黄铜矿 精铜冰铜(Cu2S和FeS)
精铜冰铜(Cu2S和FeS) 粗铜
粗铜 精铜
精铜
(4)“还原”工艺中其中一个反应为:Cu2S+2Cu2O  6Cu+SO2↑,该反应的氧化剂是 .
6Cu+SO2↑,该反应的氧化剂是 .
(5)粗铜含少量Fe、Ag、Au等金属杂质,电解精炼铜时,阴极反应式为 .完成图2中由粗铜电解得到精铜 的示意图,并作相应标注.
的示意图,并作相应标注.

查看答案和解析>>
科目:高中化学 来源:2016届宁夏回族自治区银川一中高三上学期第二次月考化学试卷(解析版) 题型:推断题
(14分)已知A~K所代表的各物质都是中学化学里常见的物质,且I是具有磁性的物质,D和K都具有两性。一定条件下,各物质间的相互反应转化关系如下图所示:
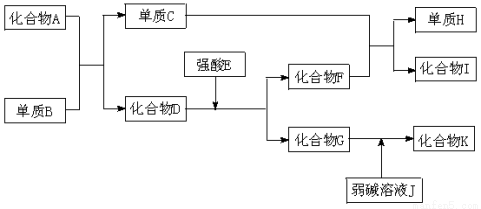
请回答:
(1)写出有关物质化学式:D是 ,H是 。
(2)写出下列反应的方程式:
①化合物G的溶液呈 (酸性,碱性,中性),其原因用离子方程式表示为 ,
②写出C+F H+I的化学方程式并用单线桥表示反应过程中电子转移的方向和数目 。
H+I的化学方程式并用单线桥表示反应过程中电子转移的方向和数目 。
③G+J K用离子方程式表示为 。
K用离子方程式表示为 。
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
利用下列各组物质制备和收集少量相应气体,能采用下图实验装置的是
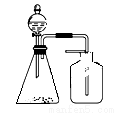
A.FeS与稀硫酸 B.铜与浓硫酸
C.稀硝酸与铜片 D.电石与水
查看答案和解析>>
科目:高中化学 来源:2016届贵州省遵义市高三上学期第一次月考化学试卷(解析版) 题型:选择题
反应(1)、(2)分别是从海藻灰和智利硝石中提取碘的主要反应:
(1)2NaI+MnO2+3H2SO4====2NaHSO4+MnSO4+2H2O+I2
(2)2NaIO3+5NaHSO3====2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是
A.两个反应中NaHSO4均为氧化产物
B.I2在反应(1)中是还原产物,在反应(2)中是氧化产物
C.氧化性:MnO2>SO42->IO3- >I2
D.反应(1)、(2)中生成等量的I2时转移电子数之比为1∶5
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁葫芦岛一中高二上期初考试化学试卷 (解析版) 题型:填空题
(11分)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为 ;
(2)从开始至2min,Z的平均反应速率为 ;
(3)若X、Y、Z均为气体,反应达平衡时:
①此时体系的压强是开始时的 倍;
②若此时只将容器的体积扩大为原来的2倍,达新平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应为 反应(填“放热”或“吸热”);达新平衡时,容器内混合气体的平均分子量比原平衡时 (填增大、减小或相等)。
(4)此反应达平衡后,若只加大体系压强,Z的物质的量减少,若Y是气体,则X的聚集状态是 。
查看答案和解析>>
科目:高中化学 来源:2016届广西河池市高三上学期第一次月考理综化学试卷(解析版) 题型:实验题
(14分)“侯氏制碱法”是我国著名的工业化学家侯德榜发明的,该制碱法为中国化学工业乃至世界化学工业做出了重要的贡献。请回答以下问题:
(1)为了验证NaHCO3和Na2CO3的稳定性,设计了如图的实验装置(铁架台、夹持仪器、加热装置等已省略):
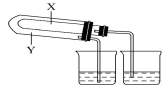
在Y中应放的物质是 (填化学式)。
(2)某化学研究性学习小组以NH3、CO2、饱和食盐水为原料,模拟侯德榜先生制碱原理设计了下图的实验装置。

①写出对应仪器的名称:a ,b 。
②实验的操作步骤中,打开旋塞K1、K2的合理顺序为:先打开 ,后打开 (填字母代号)。理由是 。
③利用该装置制得的NaHCO3将采用 (填实验操作)分离;
装置中气胆的作用是 。
(3)实验室欲配制500mL0.1 mol·L-1NaHCO3溶液。
①配制溶液时需用的玻璃仪器主要有量筒、烧杯、玻璃棒、 、 。
②下列情况会造成所配溶液的浓度偏低的是
a.加水时超过刻度线 b.容量瓶内壁附有水珠而未干燥处理
c.未洗涤烧杯和玻璃棒 d.定容时俯视刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com