
【题目】以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如图1: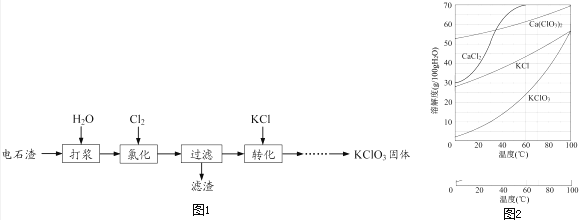
(1)氯化过程控制电石渣过量,在75℃左右进行.氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2 , 少量Ca(ClO)2 分解为CaCl2和O2 .
①生成Ca(ClO)2的化学方程式为 .
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有(填序号).
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2 转化为Ca(ClO3)2的总反应方程式为:
6Ca(OH)2+6Cl2═Ca(ClO3)2+5CaCl2+6H2O
氯化完成后过滤.
①滤渣的主要成分为(填化学式).
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2]:n[CaCl2]1:5(填“>”、“<”或“=”).
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3 , 若溶液中KClO3的含量为100gL﹣1 , 从该溶液中尽可能多地析出KClO3固体的方法是 .
【答案】
(1)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;AB
(2)CaCO3、Ca(OH)2;<
(3)蒸发浓缩、冷却结晶
【解析】电石渣含有Ca(OH)2 , 加入水打浆,通入氯气,可生成Ca(ClO)2 , Ca(ClO)2进一步转化为Ca(ClO3)2 , 过滤后在滤液中加入KCl转化生成KClO3 , 经蒸发浓缩、冷却结晶可得晶体KClO3。
(1)①氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
②提高Cl2转化为Ca(ClO3)2的转化率,可使氯气和氢氧化钙充分接触,可适当减缓通入Cl2速率、充分搅拌浆料,因氢氧化钙微溶于水,加水溶解的做法不可取,因浓度过低,对后续实验不利,故答案为:AB;
(2)①发生6Ca(OH)2+6Cl2═Ca(ClO3)2+5CaCl2+6H2O,生成的Ca(ClO3)2溶于水,CaCO3不溶于水,Ca(OH)2微溶,则滤渣中含有CaCO3、Ca(OH)2 , 故答案为:CaCO3、Ca(OH)2;
②氯化过程中Cl2与氢氧化钙反应部分生成Ca(ClO)2和CaCl2 , 则n[Ca(ClO3)2]:n[CaCl2]<1:5,故答案为:<;
(3)该溶液中尽可能多地析出KClO3固体,应经蒸发浓缩、冷却结晶,故答案为:蒸发浓缩、冷却结晶.
本题考查物质的制备,为高考常见题型和高频考点,侧重于考查学生的分析、实验能力,解答本题注意把握物质的性质以及题给信息,把握反应的流程,同时要具有扎实的实验基础知识,难度不大.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质的制备和转化正确的是
A.常温下,用铝与浓硫酸反应制备二氧化硫
B.氯化钡溶液中通入二氧化硫可生成BaSO3沉淀
C.用FeS除去废水中的重金属铜离子
D.以粗铜作阴极,硫酸铜溶液为电解质溶液电解精炼铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种医药中间体,其结构简式如图所示.下列有关化合物X的说法正确的是( ) 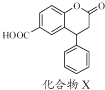
A.分子中两个苯环一定处于同一平面
B.不能与饱和Na2CO3溶液反应
C.在酸性条件下水解,水解产物只有一种
D.1 mol化合物X最多能与2 molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)2Z(g),此反应达到平衡的标志是( )
A.容器内气体密度不随时间变化
B.v(X):v(Y)=1:2
C.容器内X、Y、Z的浓度不随时间变化
D.单位时间消耗0.1molX同时生成0.2molZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有25mL 2molL﹣1 Na2CO3和75mL 1molL﹣1的稀盐酸:①将Na2CO3溶液缓缓滴到稀盐酸中 ②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况是( )
A.均为0.84 L
B.均为0.56 L
C.①>②
D.②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是合成抗心律失常药物泰达隆的一种中间体,可通过以下方法合成: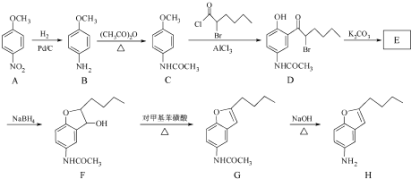
(1)D中的含氧官能团名称为(写两种).
(2)F→G的反应类型为 .
(3)写出同时满足下列条件的C的一种同分异构体的结构简式 .
①能发生银镜反应;
②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应;
③分子中只有4种不同化学环境的氢.
(4)E经还原得到F,E的分子是为C14H17O3N,写出E的结构简式 .
(5)已知:①苯胺( ![]() )易被氧化
)易被氧化 ![]() 请以甲苯和(CH3CO)2O为原料制备
请以甲苯和(CH3CO)2O为原料制备 ![]() ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL FeI2溶液中逐渐通入Cl2 , 会依次生成Cl﹣、I2、Fe3+、IO3﹣ , 其中Fe3+、I2的物质的量随n(Cl2)的变化如图所示,请回答下列问题: 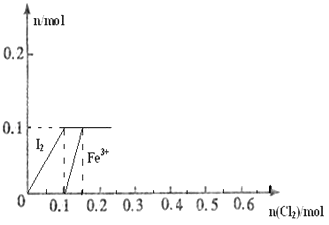
(1)由图可知,I﹣、Fe2+、I2三种粒子的还原性由强到弱的顺序为>> .
(2)当n(Cl2)=0.12mol时,溶液中的离子主要为 , 从开始通入Cl2到n(Cl2)=0.12mol时的总反应的化学方程式为 .
(3)当溶液中n(Cl﹣):n(IO3﹣)=8:1时,通入的Cl2在标准状况下的体积为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从能量的变化和反应的快慢等角度研究反应:2H2+O2=2H2O.
(1)为了加快反应速率,不可以采取的措施有(填序号,下同). A.使用催化剂 B.提高氧气的浓度
C.提高反应的温度 D.降低反应的温度
(2)已知该反应为放热反应,如图能正确表示该反应中能量变化的是 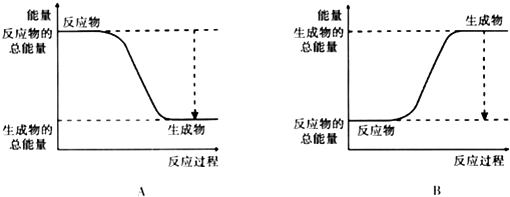
(3)从断键和成键的角度分析上述反应中能量的变化.已知化学键的键能如表:
化学键 | H﹣H | O=O | H﹣O |
键能kJmol﹣1 | 436 | 496 | 463 |
由此计算2mol H2在氧气中燃烧生成气态水放出的热量 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于吸热反应的是( )
A.C6H12O6(葡萄糖)+6O2═6CO2+6H2O
B.CH3COOH+KOH═CH3COOK+H2O
C.所有高温条件下发生的反应
D.C+CO2 ![]() 2CO
2CO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com