
分析 乙烯含有双键,能与溴水发生加成反应,乙烯和乙烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了5.6g,即为乙烯的质量.根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$计算物质的量、质量关系.
解答 解:11.2L混合气体的物质的量为n=$\frac{V}{{V}_{m}}$=$\frac{11.2L}{22.4L/mol}$=0.5mol,
乙烯含有双键,能与溴水发生加成反应,乙烯和乙烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了5.6g,即为乙烯的质量,
所以乙烯的物质的量为n=$\frac{m}{M}$=$\frac{5.6g}{28g/mol}$=0.2mol,
则乙烷的物质的量为:0.5mol-0.2mol=0.3mol,质量为:0.3mol×30g/mol=9g,
所以,乙烯与乙烷的物质的量之比为0.2mol:0.3mol=2:3,
质量之比为5.6g:9g=28:45,
答:原气体混合物中乙烯与乙烷的物质的量之比和质量比分别为2:3、28:45.
点评 本题考查物质的量的相关计算,题目难度不大,注意乙烯与乙烷的性质差别.


科目:高中化学 来源: 题型:选择题
| A. | Li2NH中N的化合价是-1 | B. | LiH的电子式为Li+:H- | ||
| C. | 该反应中H2既是氧化剂又是还原剂 | D. | LiNH2是还原产物,LiH是氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| J | ||||
| R | T |
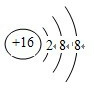 .
.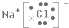 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
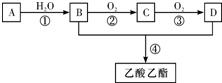
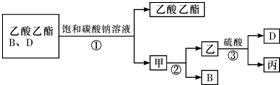
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
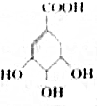 是从烹调香料“八角”提取的一种有机物,是合成抗禽流感药物的基本原料,1mol莽草酸与足量的Na和NaOH反应,消耗的Na和NaOH的物质的量之比为( )
是从烹调香料“八角”提取的一种有机物,是合成抗禽流感药物的基本原料,1mol莽草酸与足量的Na和NaOH反应,消耗的Na和NaOH的物质的量之比为( )| A. | 4:1 | B. | 1:1 | C. | 3:1 | D. | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1摩尔任何气体都含有6.02×1023个分子 | |
| B. | 0.012Kg12C中含有6.02×1023个碳原子 | |
| C. | 1摩尔水中含有2mol氢和1mol氧 | |
| D. | 1molH2O中含有3 mol原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com