
【题目】下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O
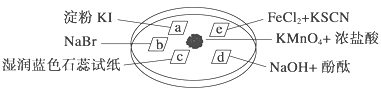
对实验现象的“解释或结论”正确的是 ( )
选项 | 实验现象 | 解释或结论 |
A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
C | d处立即褪色 | 氯气与水生成了漂白性物质 |
D | e处变红色 | 还原性:Fe2+>Cl- |
A. A B. B C. C D. D
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】氨氮废水中的氮元素多以NH4+和NH3H2O的形式存在.某工厂处理氨氮废水的流程如下: 含NH4+的废水 ![]() 低浓度氨氮废水
低浓度氨氮废水 ![]() 含余氯废水
含余氯废水 ![]() 达标废水
达标废水
(1)I中加入NaOH溶液,调pH=11并鼓入大量空气.用离子方程式表示加NaOH溶液的作用是;鼓入大量空气的目的是 .
(2)II中加入适量NaClO溶液,控制pH在6~7,将氨氮转化为无毒物质. ①为了完全从废水中去除氨氮,加入的NaClO与水体中NH4+的物质的量之比最小是 .
②过程 II发生3个反应:
i.ClO﹣+H+═HClO
ii.NH4++HClO═NH2Cl+H++H2O (NH2Cl中Cl元素为+1价)
iii. …
已知:水体中以+1价形式存在的氯元素有消毒杀菌的作用,被称为“余氯”.图为NaClO加入量与“余氯”含量的关系示意图.其中氨氮含量最低的点是c点.
b点表示的溶液中氮元素的主要存在形式是(用化学式表示);反应iii的化学方程式是 . 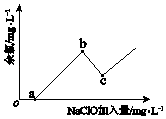
(3)III中用Na2SO3溶液处理含余氯废水,要求达标废水中剩余Na2SO3的含量小于5mgL﹣1 . 若含余氯废水中NaClO的含量是7.45mgL﹣1 , 则处理10m3含余氯废水,至多添加10% Na2SO3溶液kg(溶液体积变化忽略不计).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中乙是甲的电解池进行电解时的某个量(纵坐标x)随时间变化的曲线(各电解池都用石墨作电极,不考虑电解过程中溶液浓度变化对电极反应的影响),则x表示( ) 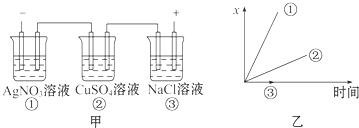
A.各电解池析出气体体积总数的变化
B.各电解池阳极质量的增加
C.各电解池阴极质量的增加
D.各电极上放电的离子总数的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据下图中氮元素及其化合物的转化关系,回答问题:
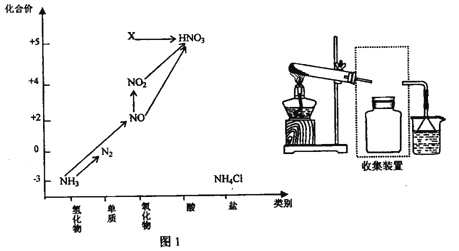
(1)实验窒常用NH4Cl 与Ca(OH)2制取氨气,该反应的化学方程式为___________。
(2)若要收集一瓶氨气,请将下列装置补充完整,在虚框内画出连接图。___________
(3)下列试剂不能用手干燥NH3的是_________。
A.浓硫酸 B.碱石灰 C.NaOH 固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO 化学方程式为____________。
②NO→NO2 实验现象是_______ 。
③ NO2![]() HNO3 氧 化剂 与 还原剂物质的量之比为_______。
HNO3 氧 化剂 与 还原剂物质的量之比为_______。
(5)图1中,实验室只用一种物质将NO 直接转化为硝酸且绿色环保,则该物质的化学式为_____________,
(6) 图1中,X的化学式为__________,从物质性质上看,X 属于_______氧化物。
(7)若要将NH3→N2,,从原理上看,下列试剂可行的是_______。
A.O2 B.Na C.NH4Cl D.NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O ![]() Cd(OH)2+2Ni(OH)2有关其说法正确的是( )
Cd(OH)2+2Ni(OH)2有关其说法正确的是( )
A.充电过程是化学能转化为电能的过程
B.放电时负极附近溶液的碱性不变
C.放电时电解质溶液中的OH﹣向正极移动
D.充电时阳极反应:Ni(OH)2﹣e﹣+OH﹣=NiOOH+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述中,正确的是
①新制氯水久置后→浅黄绿色消失
②淀粉溶液遇单质碘→蓝色
③蔗糖中加入浓硫酸搅拌→白色
④SO2通入品红溶液中→红色褪去
⑤氨气通入酚酞溶液中→红色
⑥用稀盐酸酸化Fe(NO3)2→变黄
⑦浓硝酸涂在蓝色石蕊试纸→变红
⑧Fe(OH)3胶体通电一段时间→正极附近颜色加深
A.①②③④⑥ B.②③④⑤⑦ C.①②④⑤⑥ D.①③④⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.常温常压下,1mol丙烷共用电子对数为10 NA
B.0.5 mol甲烷和0.5 mol乙酸完全燃烧消耗的O2分子数都为0.2NA
C.标准状况下,1L辛烷充分燃烧后生成气态产物的分子数为 ![]() NA
NA
D.1 mol甲醇与足量钠反应,转移电子数目为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA表示阿伏伽德罗常数,则关于热化学方程式:C2H2(g)+ ![]() O2(g)═2CO2(g)+H2O(l)△H=﹣1300kJmol﹣1的说法中,正确的是( )
O2(g)═2CO2(g)+H2O(l)△H=﹣1300kJmol﹣1的说法中,正确的是( )
A.当有6 NA个电子转移时,该反应放出1300 kJ的能量
B.当有NA个水分子生成且为液体时,吸收1300 kJ的能量
C.当有4NA个碳氧共用电子对生成时,放出1300 kJ的能量
D.当有8NA个碳氧共用电子对生成时,放出1300 kJ的能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com