
【题目】aL体积比为1∶3的A、B两种链烃的混合气体,可与0.5aL(状态相同)氢气发生加成反应,则A、B两种链烃的通式可能是( )
A. CnH2n-2和CnH2n+2B. C nH2n和CnH2n+2
C. CnH2n和CnH2nD. CnH2n和CnH2n-2
【答案】A
【解析】
链烃通常可分为烷、烯、炔三大类,烷烃无法发生加成反应,单烯烃与氢气一比一加成(物质的量之比),单炔烃与氢气一比二加成(物质的量之比)。A、B两种链烃的混合气体aL体中,A占总体积的![]() ,B占总体积的
,B占总体积的![]() 。
。
A.![]() aLCnH2n-2与0.5aL氢气反应,CnH2n+2不与氢气反应,消耗氢气0.5aL,A项正确;
aLCnH2n-2与0.5aL氢气反应,CnH2n+2不与氢气反应,消耗氢气0.5aL,A项正确;
B.![]() aLCnH2n与
aLCnH2n与![]() aL氢气反应,CnH2n+2不与氢气反应,所以混合气体共消耗氢气
aL氢气反应,CnH2n+2不与氢气反应,所以混合气体共消耗氢气![]() aL,与题给的数据不符,B项错误;
aL,与题给的数据不符,B项错误;
C.![]() aLCnH2n与
aLCnH2n与![]() aL氢气反应,
aL氢气反应,![]() aLCnH2n与0.75aL氢气反应,消耗氢气aL,与题给的数据不符,C项错误;
aLCnH2n与0.75aL氢气反应,消耗氢气aL,与题给的数据不符,C项错误;
D.![]() aLCnH2n与
aLCnH2n与![]() aL氢气反应,
aL氢气反应,![]() aLCnH2n-2与1.5aL氢气反应,消耗氢气1.75aL ,与题给的数据不符,D项错误;
aLCnH2n-2与1.5aL氢气反应,消耗氢气1.75aL ,与题给的数据不符,D项错误;
所以答案选择A项。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
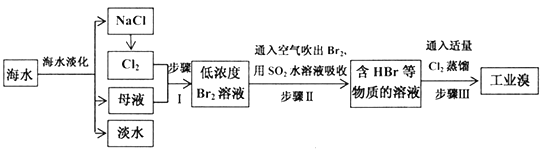
(1)写出步骤I中生成低浓度Br2的离子方程式______。
(2)步骤I中已获得Br2,步骤I中又将Br2还原为Br-,其目的为富集溴元素,请写出步骤II的化学方程式_______。
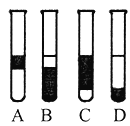
(3)在3mL溴水中加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象为如图中的_______。
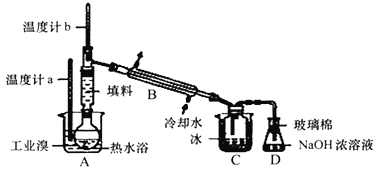
(4)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料:Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性,他们设计了如图装置简图。请你参与分析讨论:
①C中液体产物颜色为_____。
②用离子方程式解释NaOH浓溶液的作用______。
查看答案和解析>>
科目:高中化学 来源: 题型:
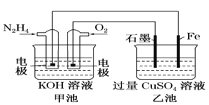
【题目】(1)下图中甲池的总反应式为N2H4+O2===N2+2H2O。甲池中负极上的电极反应式为_________,乙池中石墨电极上发生的反应为_______________。甲池中每消耗0.1 mol N2H4,乙池电极上则会析出_________ g固体。
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。下图为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。E为该燃料电池的_______极(填“正”或“负”)。F电极上的电极反应式为______________。

(3)下图为电化学法生产硫酸的工艺示意图,电池以固体金属氧化物作电解质,该电解质能传导O2-离子。S(g)在负极生成SO3的电极反应式为____________________。已知S(g)在负极发生的反应为可逆反应,为提高硫蒸气的转化率,该工艺采取的措施有____________(任写一条)。
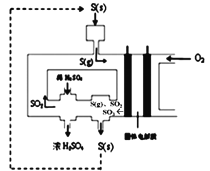
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X元素的1个原子失去2个电子转移到Y元素的2个原子中去,形成离子化合物Z,下列说法中不正确的是( )
A. Z在熔化状态下可以导电B. Z可以表示为XY2
C. X形成+2价阳离子D. Z中存在共价键,Z可以电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理加以解释的是
A. 夏天,打开啤酒瓶时会在瓶口逸出气体
B. 浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体
C. 压缩氢气与碘蒸气反应的平衡混合气体,颜色变深
D. 将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀H2SO4、NaOH溶液等试剂)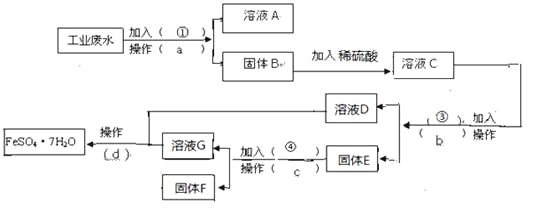
(1)操作a的名称为___________,所需要的玻璃仪器为________________________。
(2)固体E的成分为_________________,加入的试剂④为________________,发生的化学方程式为__________________________________________。
(3)加入试剂①的目的是______________________________________________________。
(4)从溶液D和溶液G中得到FeSO4.7H2O晶体的操作为_____________、冷却结晶、________、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,二甲胺[(CH3)2NH·H2O]是一元弱碱,其电离常数Kb=1.6×10-4。10 mL c mol·L-1二甲胺溶液中滴加0.1mo1·L-1盐酸,混合溶液的温度与盐酸体积的关系如图所示。下列说法不正确的

A. 二甲胺溶液的浓度为0.2mol·L-1
B. 在Y和Z点之间某点溶液pH=7
C. Y点存在:c(Cl-)>c[(CH3)2NH2+]>c(H+)>c(OH-)
D. 常温下,(CH3)2NH2Cl水解常数Kh≈5.0×10-11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如右图所示。下列分析不正确的是( )

A. ①代表滴加H2SO4溶液的变化曲线
B. b点,溶液中大量存在的离子是Na+、OH–
C. c点,两溶液中含有相同量的OH–
D. a、d两点对应的溶液均显中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com