
| 选项 | X | Y | 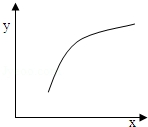 |
| A | 温度 | 容器内混合气体的密度 | |
| B | A的物质的量 | B的转化率 | |
| C | 催化剂的质量 | C的体积分数 | |
| D | 加入Ar的物质的量 | 逆反应速率 |
| A. | A | B. | B | C. | C | D. | D |
分析 反应2A(g)+B(g)$\frac{\underline{\;催化剂\;}}{\;}$3C(g);△H<0,平衡常数只随温度变化,增加B的量,促进A的转化,加入C,化学平衡逆向移动,增大压强,平衡正向移动,升高温度,化学平衡逆向移动,催化剂改变反应速率不改变化学平衡,结合图象可知一个量增大引起另一个量的增大来解答.
解答 解:A.达平衡后,升高温度,化学平衡逆向移动,反应前后气体体积、质量不变,密度始终不变,与图象不符合,故A错误;
B.达平衡后,加入A的物质的量,平衡正向移动,则B的转化率增大,与图象符合,故B正确;
C.达平衡后,再加入催化剂,改变化学反应速率,化学平衡不移动,C的体积分数不变,与图象不符合,故C错误;
D.加入惰性气体,平衡不移动,故D错误.
故选B.
点评 本题考查化学平衡的影响因素及化学平衡图象,为高频考点,侧重于学生的分析能力的考查,明确不同因素对化学平衡的影响及由图象得出一个量增大引起另一个量的增大是解答本题的关键,题目难度中等.


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
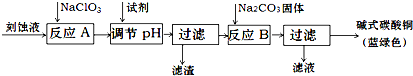
| 物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com