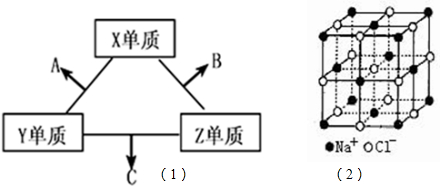
��2013?����һģ��Ŀǰ��ҵ����һ����CO
2������ȼ�ϼ״��ķ��������Խ�CO
2�������
��1����֪�ڳ��³�ѹ�£�
��2CH
3OH��l��+3O
2��g��=2CO
2��g��+4H
2O��g����H=
_1275.6kJ?mol
-1��2CO��g��+O
2��g��=2CO
2��g����H=
_556.0kJ?mol
-1��H
2O��l��=H
2O��g����H=+44.0kJ?mol
-1д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ
CH3OH��l��+O2��g��=CO ��g��+2H2O��l����H=_447.8 kJ?mol-1
CH3OH��l��+O2��g��=CO ��g��+2H2O��l����H=_447.8 kJ?mol-1
��2��ijͬѧ���ü״�ȼ�ϵ��Ϊ��Դ�������һ�ֵ�ⷨ��ȡFe��OH��
2��ʵ��װ�ã���ͼ����ͨ�����Һ�в��������İ�ɫ�������ҽϳ�ʱ�䲻��ɫ�����Դ��a��Ϊ
��
��
�������������������缫��ӦʽΪ
O2+4e-+2H2O=4OH-
O2+4e-+2H2O=4OH-
��װ���϶�A���缫������
Fe
Fe
���ѧʽ����B�缫�ϵĵ缫��ӦʽΪ
2H++2 e-=H2��
2H++2 e-=H2��
��
��3������ͬ����CO��g����H
2O��g���ֱ�ͨ�����Ϊ2L�ĺ����ܱ������У����з�Ӧ��CO��g��+H
2O��g��?CO
2��g��+H
2��g�����õ������������ݣ�
| ʵ���� |
�¶�/�� |
��ʼ��/mol |
ƽ����/mol |
�ﵽƽ������ʱ��/min |
| H2O |
CO |
CO2 |
| 1 |
650 |
2 |
4 |
1.6 |
5 |
| 2 |
900 |
1 |
2 |
0.4 |
3 |
| 3 |
900 |
1 |
2 |
0.4 |
1 |
�ٸ÷�Ӧ������ӦΪ
��
��
��������š����ȷ�Ӧ��
��ʵ��1�У���v��H
2����ʾ��ƽ����Ӧ����Ϊ
0.16mol/��L?min��
0.16mol/��L?min��
��
��900��ʱ����CO��g����H
2O��g����CO
2��g�� �� H
2��g�������ʵ����ֱ���0.8mol��1.0mol��0.6mol��0.8mol�ֱ��������������ʱ��Ӧ��v������
��
��
v���棩���������������=����֮һ����
��ʵ��3��ʵ��2��ȣ��ı������������
ʹ���˴������Ӵ���ѹǿ
ʹ���˴������Ӵ���ѹǿ
��

 ��2013?����һģ��Ŀǰ��ҵ����һ����CO2������ȼ�ϼ״��ķ��������Խ�CO2���Ϊ����
��2013?����һģ��Ŀǰ��ҵ����һ����CO2������ȼ�ϼ״��ķ��������Խ�CO2���Ϊ����