
【题目】物质G是制备抗癌药物吉非替尼过程中重要的中间体,某研究小组按照下列线路合成中间体G。

已知: 、
、 、
、 (同时还有H2O或卤化氢生成)
(同时还有H2O或卤化氢生成)
请回答:
(1)下列说法正确的是_______。
A.化合物A能够使酸性高锰酸钾溶液褪色
B.化合物A中含有4种不同的官能团
C.化合物C具有碱性
D.化合物G的分子式为C15H20N3O3
(2)上述路线中合成A的反应类型为______,化合物E的结构简式为______。
(3)写出C到D的化学反应方程式________。
(4)请设计以乙烯为原料转变为物质C的合成线路(用流程图表示,无机试剂任选)___。
(5)写出化合物B(C8H7NO2)可能的同分异构体_______。须同时满足:①能发生银镜反应;②1H—NMR谱显示分子中含有苯环,且分子中有4种不同化学环境的氢原子。
【答案】AC 取代反应 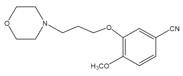
![]() 或
或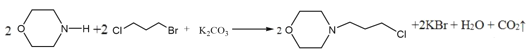 CH2=CH2
CH2=CH2![]() CH2Br-CH2Br
CH2Br-CH2Br![]() CH2OHCH2OH
CH2OHCH2OH![]() HOCH2CH2OCH2CH2OH
HOCH2CH2OCH2CH2OH![]()
![]()
 、
、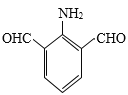 、
、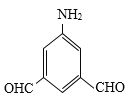 、
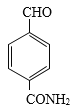
、
【解析】
物质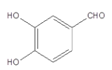 与CH3I发生碘仿反应产生物质A结构简式是:
与CH3I发生碘仿反应产生物质A结构简式是: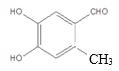 ,
, 与①NH2OH/HCl、②CH3COCl/CCl4作用,可得B:
与①NH2OH/HCl、②CH3COCl/CCl4作用,可得B: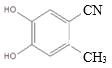 ;由于物质在转化过程中结构不变,所以根据物质转化关系,由G结构可知分子式是C4H9NO的物质C结构简式是
;由于物质在转化过程中结构不变,所以根据物质转化关系,由G结构可知分子式是C4H9NO的物质C结构简式是![]() ,C与BrCH2CH2CH2Cl在K2CO3作用下发生反应产生D为
,C与BrCH2CH2CH2Cl在K2CO3作用下发生反应产生D为![]() ,B与D反应产生E是
,B与D反应产生E是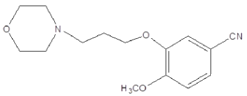 ,E与浓HNO3、浓H2SO4共热,发生硝化反应,产生F:
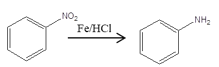
,E与浓HNO3、浓H2SO4共热,发生硝化反应,产生F: ,F在Fe/HCl存在条件下发生还原反应产生G:
,F在Fe/HCl存在条件下发生还原反应产生G: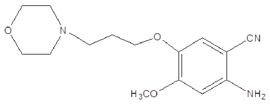 。
。
(1)物质A是 ,该物质含有酚羟基、醛基,甲基,因此可以被酸性
,该物质含有酚羟基、醛基,甲基,因此可以被酸性
B.根据A的结构简式可知A含有酚羟基-OH、醛基-CHO两种官能团,B错误;
C.化合物C结构简式是![]() ,含有碱性基团
,含有碱性基团![]() ,因此该物质具有碱性,C正确;
,因此该物质具有碱性,C正确;
D.根据化合物G的结构简式,结合C原子价电子是4个的原则,可知G分子式是C15H21N3O3,D错误;
故合理选项是AC;
(2)物质 与CH3I发生碘仿反应产生物质A
与CH3I发生碘仿反应产生物质A ,所以合成A物质的反应属于取代反应;根据上述推断可知:化合物E结构简式为
,所以合成A物质的反应属于取代反应;根据上述推断可知:化合物E结构简式为 ;
;
(3)物质C是![]() ,C与BrCH2CH2CH2Cl在K2CO3作用下发生反应产生D
,C与BrCH2CH2CH2Cl在K2CO3作用下发生反应产生D![]() ,该反应的化学方程式为:
,该反应的化学方程式为:![]() ,或
,或
 ;
;
(4)乙烯CH2=CH2通入Br2水中发生加成反应产生1,2-二溴乙烷CH2Br-CH2Br, CH2Br-CH2Br与NaOH的水溶液共热,发生取代反应产生 CH2OHCH2OH,CH2OHCH2OH与浓硫酸共热,发生分子间的取代反应产生HOCH2CH2OCH2CH2OH,该物质与NH3反应产生![]() ,所以以乙烯为原料转变为物质 C 的合成线路是CH2=CH2
,所以以乙烯为原料转变为物质 C 的合成线路是CH2=CH2![]() CH2Br-CH2Br
CH2Br-CH2Br![]() CH2OHCH2OH
CH2OHCH2OH![]() HOCH2CH2OCH2CH2OH
HOCH2CH2OCH2CH2OH![]()
![]() ;
;
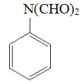
(5)物质B是 ,分子式为C8H7NO2,其同分异构体满足条件:①能发生银镜反应,说明分子中含有醛基-CHO;②1H—NMR 谱显示分子中含有苯环,且分子中有 4 种不同化学环境的氢原子,则符合题意的物质结构简式为:
,分子式为C8H7NO2,其同分异构体满足条件:①能发生银镜反应,说明分子中含有醛基-CHO;②1H—NMR 谱显示分子中含有苯环,且分子中有 4 种不同化学环境的氢原子,则符合题意的物质结构简式为: 、
、 、
、 、
、 。
。


科目:高中化学 来源: 题型:
【题目】常温时,改变饱和氯水的pH,得到部分含氯微粒的物质的量分数与pH的关系如图所示。下列叙述不正确的是
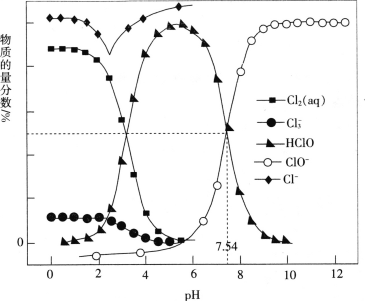
A.pH=1的氯水中,c(Cl2)>c(Cl3-)>c(HClO)>c(ClO-)
B.氯水中的Cl2、ClO-、HClO均能与K2S发生反应
C.已知常温下反应Cl2(aq)+Cl-(aq)![]() Cl3- (aq)的K=0.191,当pH增大时,K减小
Cl3- (aq)的K=0.191,当pH增大时,K减小
D.该温度下,HClO![]() H++ClO-的电离常数Ka=10-7.54
H++ClO-的电离常数Ka=10-7.54
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B的产量可以衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示![]() 部分反应条件、产物省略
部分反应条件、产物省略![]() :
:
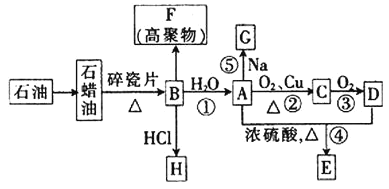
回答下列问题:
![]() 工业上,由石油获得石蜡油的方法称为_________,由石蜡油获得B的方法称为__________。
工业上,由石油获得石蜡油的方法称为_________,由石蜡油获得B的方法称为__________。
![]() ①决定化合物A的化学特性的原子团的名称为______________。
①决定化合物A的化学特性的原子团的名称为______________。
②![]() 到A的反应类型为_______,A到E的反应类型为____________。
到A的反应类型为_______,A到E的反应类型为____________。
③![]() 的分子式为_________;F的结构简式为___________。
的分子式为_________;F的结构简式为___________。
![]() 写出下列反应的化学方程式。
写出下列反应的化学方程式。
反应①:___________________________________________________;
反应②:___________________________________________________;
反应⑤:___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素铬(Cr)的几种化合物存在下列转化关系,下列判断不正确的是
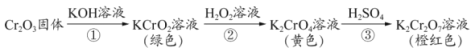
A.反应①表明Cr2O3有酸性氧化物的性质
B.反应②利用了H2O2的氧化性
C.反应②的离子方程式为2CrO2ˉ+3H2O2+2OHˉ=2CrO42ˉ+4H2O
D.反应①②③中铬元素的化合价均发生了变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化合物X仅由三种短周期元素组成,X隔绝空气加热,可分解为盐A和气体B,有关该反应的物质转换、现象和量的关系如下图所示。

(1)检验盐A中阳离子的方法及现象是____________。
(2)请用双桥法分析并表达化合物X分解时,电子转移的方向和数目____________。
(3)白色沉淀C在紫外光照射下会发生分解,请写出该反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
①Zn为正极,Cu为负极;
②H+向负极移动;
③电子是由Zn经外电路流向Cu;
④Cu极上有H2产生;
⑤若有1mol电子流过导线,则产生的H2为0.5mol;
⑥正极的电极反应式为Zn﹣2e﹣═Zn2+.

A.①②③ B.③④⑤ C.④⑤⑥ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素位于短周期,原子序数依次增大,C基态原子核外有三个未成对电子,B与D形成的化合物BD与C的单质C2电子总数相等,CA3分子结构为三角锥形,D与E可形成E2D与E2D2两种离子化合物,D与F是同族元素。根据以上信息,回答下列有关问题:
(1)写出基态时D的电子排布图________。
(2)写出化合物E2F2的电子式________,化合物ABC的结构式________。
(3)根据题目要求完成以下填空:
①BF32﹣中心原子杂化方式________;CA3中心原子杂化方式________;
②FD42﹣微粒中的键角________; FD3分子的立体构型________。
(4)F元素两种氧化物对应的水化物酸性由强到弱为__________,原因__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示的反应路线及所给信息填空。

(1)A的名称是____________________![]() 中官能团名称是______________。
中官能团名称是______________。
(2)的反应类型是________________。
(3)反应④的化学方程式是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10L密闭容器中,1molA和3molB在一定条件下反应:A(g)+xB(g)![]() 2C(g),2min后反应达到平衡时,测得混合气体共3.4mol,生成0.4molC,则下列计算结果不正确的是( )
2C(g),2min后反应达到平衡时,测得混合气体共3.4mol,生成0.4molC,则下列计算结果不正确的是( )
A.平衡时,物质的量比A:B:C=2:11:4
B.x值等于4
C.A的转化率20%
D.B的平均反应速率为0.04mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com